对于反应:A+B=C下列条件的改变一定能使化学反应速率加快的 是 ( )
是 ( )
| A.升高体系的温度 | B.增加A的物质的量 |
| C.增加体系的压强 | D.减少C的物质的量浓度 |
在恒温条件下,有甲、乙两容器,甲容器为体积不变的密闭容器,乙容器为一个恒压的密闭容器,两容器起始状态完全相同,都充有C气体,若发生可逆反应

 ,经一段时间后,甲、乙两容器反应都达到平衡,下列说法中正确的是
,经一段时间后,甲、乙两容器反应都达到平衡,下列说法中正确的是
A.平均反应速度: |
B.平衡时C的物质的量甲>乙 |
| C.平衡时C的转化率:乙<甲 | D.平衡时A的物质的量甲>乙 |
25℃时将水不断滴入 的氨水中,下列变化的图象合理的是
的氨水中,下列变化的图象合理的是
容积固定的密闭容器中存在如下反应: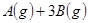

 ,△H
,△H 。某研究小组研究了其他条件不变时,改变某一条件对上述反应的影响,并根据实验数据作出下列关系图:
。某研究小组研究了其他条件不变时,改变某一条件对上述反应的影响,并根据实验数据作出下列关系图:
下列判断一定错误的是
①图I研究的是不同催化剂对反应的影响,且乙使用的催化剂效率较高
②图II研究的是压强对反应的影响,且甲的压强较高
③图II研究的是温度对反应的影响,且甲的温度较高
④图III研究的是不同催化剂对反应的影响,且甲使用的催化剂效率较高
| A.①② | B.①③ | C.②④ | D.③④ |
在一密闭烧瓶中,在25℃时存在着平衡:

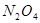 (正反应放热)。把烧瓶置于100℃的水中,则下列几项性质中不会改变的是
(正反应放热)。把烧瓶置于100℃的水中,则下列几项性质中不会改变的是
①颜色;②平均分子量;③质量;④压强;⑤密度
| A.①和③ | B.②和④ | C.④和⑤ | D.③和⑤ |
已知298K时,

 ,△H
,△H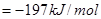 ,在相同温度下,向固定体积的密闭容器中通入
,在相同温度下,向固定体积的密闭容器中通入 和
和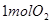 ,达到平衡时放出热量
,达到平衡时放出热量 ;向另一个同体积的密闭容器中通入
;向另一个同体积的密闭容器中通入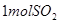 和
和 ,达到平衡时放出热量为
,达到平衡时放出热量为 ,则下列关系中正确的是
,则下列关系中正确的是
A. |
B. |
C. |
D.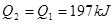 |