盐酸、硫酸和硝酸是中学阶段常见的三种强酸。请就三者与金属铜的反应情况,回答下列问题:
(1)①在100mL 1 8 mol·L-1的浓硫酸中加入过量的铜片,加热使之充分反应,产生的气体在标准状况下的体积可能是
| A.40.32L | B.30.24L | C.20.16L | D.6.72L |
②有同学提出,若使上述反应①中剩余的铜片继续溶解,可向其中加入硝酸钠,请判断该方案是否可行?若 不可行,请说明原因。若可行,请写出反应的离子方程式: 。
不可行,请说明原因。若可行,请写出反应的离子方程式: 。
(2)若将6.4g铜粉与一定量浓硝酸反应,当铜粉完全溶解时,生成气体(NO、NO2)共2.24L(标准状况),则反应中所消耗的硝酸的物质的量为 。
(3)某同学向浸泡铜片的稀盐酸中加入H2O2后,铜片溶解,并且该反应的产物只有氯化铜和水。该反应的化学方程式为: 。
A、B、C、D为四种由短周期元素形成的化合物,它们的焰色反应均为黄色,并有下列转化关系。A中既含有离子键又含有非极性共价键,D含四种元素。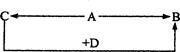
(1)A的电子式是。
(2)把1 molCO2通入含2 molC的溶液后,溶液中各离子浓度由大到小的顺序是。
(3)1 molA与2 molD固体混合后,在密闭容器中加热充分反应,排出气体物质后冷却,残留的固体是(用化学式表示)。
已知在一定条件下3分子乙炔可发生加成反应生成苯: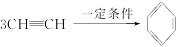
试预测下列物质3分子加成后的产物。
(1)3H—C≡ (2)3
(2)3

实验室制备硝基苯的主要步骤如下:
①配制一定比例的浓硫酸与浓硝酸的混合酸,加入反应器中。
②向室温下的混合酸中逐滴加入一定质量的苯,充分振荡,混合均匀。
③在50 ℃—60 ℃下发生反应,直至反应结束。
④除去混合酸后,粗产品依次用蒸馏水和5% NaOH溶液洗涤,最后再用蒸馏水洗涤。
⑤将用无水CaCl2干燥后的粗硝基苯进行蒸馏,得到纯硝基苯。完成下列空白:
(1)配制一定比例浓硫酸与浓硝酸混合酸时,操作注意事项是__________________________。
(2)步骤③中,为了使反应在50 ℃—60 ℃下进行,常用的方法是______________________。
(3)步骤④中洗涤、分离粗硝基苯应使用的仪器是_______________________。
(4)步骤④中粗产品用5% NaOH溶液洗涤的目的是______________________。
取0.1 mol苯的同系物完全燃烧后,生成的气体通过浓硫酸,浓硫酸增重10.8 g,再通过氢氧化钾溶液后,气体减轻39.6 g。该苯的同系物在苯环上的一氯代物、二氯代物、三氯代物分别只有一种。根据上述条件,推断它的分子式是___________,结构简式是___________,名称是___________。
有4种无色液态物质:己烯、己烷、苯和甲苯,符合下列各题要求的分别是:
(1)不能与溴水和KMnO4酸性溶液反应,但在Fe屑作用下能与液溴反应的是__________,生成的有机物名称是___________,反应化学方程式为__________,此反应属于__________反应。
(2)不与溴水和KMnO4酸性溶液反应的是___________。
(3)能与溴水和KMnO4酸性溶液反应的是___________。