( 8分) 已知:在298K、100kPa时,
①C(s,石墨)+O2(g) = CO2(g) △H1 = -400 kJ·mol-1;
②2H2(g)+O2(g) = 2H2O(l) △H2 = -570 kJ·mol-1;
③2C2H2(g)+5O2(g) = 4CO2(g)+ 2H2O(l) △H3 = -2600 kJ·mol-1;
(1)写出298K时由C(s,石墨)和H2(g)生成1 mol C2H2(g)反应的热化学方程式 。
(2)现有一定量的乙炔在足量氧气中 完全燃烧,放出热量650 kJ。将反应后的二氧化碳气体缓缓通入到含有0.5 mol Ca (OH)2的澄清石灰水中充分反应。所得溶液为 。
完全燃烧,放出热量650 kJ。将反应后的二氧化碳气体缓缓通入到含有0.5 mol Ca (OH)2的澄清石灰水中充分反应。所得溶液为 。
将反应后的溶液分为a、b两等份,分别进行下列实验,回答相应问题:
①在a中加入少量的氢氧化钠溶液,写出反应的离子方程式 。
②加热b,观察到 。
如图为以惰性电极进行电解: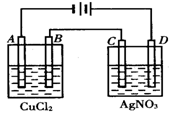
(1)写出B、C、D各电极上的电极反应式和总反应方程式:
A:________________________________,B:________________________________,
总反应方程式:________________________。
C:________________________________, D:________________________________,
总反应方程式:___________________________。
(2)在A、B、C、D各电极上析出生成物的物质的量比为__________________。
将0.1mol的铁铝混合物溶于100mL 2mol/L硫酸溶液中,然后再滴加1mol/LNaOH溶液。请回答: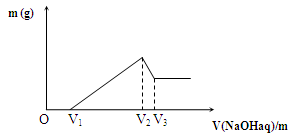
(1) 若在滴加NaOH溶液过程中,沉淀质量m随加入NaOH溶液的体积V变化如图所示。最初加入V1mLNaOH溶液的作用是_________________________;
(2)若在滴加NaOH溶液过程中,欲使Fe2+、Al3+刚好沉淀完全,则滴入NaOH溶液的体积V(NaOH)=mL。
(3)若V1=160mL,则金属混合物中n(Fe)=mol V3=mL;(写出第(2)题的解题过程)
(11分)铝土矿的主要成分是Al2O3,含有Fe2O3、SiO2等杂质,按下列操作从铝土矿中提取Al2O3。回答下列问题: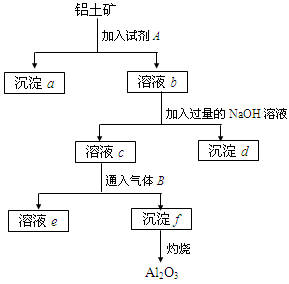
(1)沉淀物的化学式分别是:a;d ;f 。
(2)溶液b中所含的金属阳离子是;溶液c中所含的酸根离子是。
(3)加入的试剂A是,通入的气体B是,能否将B换成A?其理由是。
向FeCl3溶液中加入ag铜粉,搅拌使之全部溶解,再向其中加入 bg铁粉,充分反应后过滤得滤渣 cg,若已知 a>b>c,则 c克滤渣是_________。溶液中存在的阳离子是____ ________。
除去下表各溶液中含有的少量杂质(括号内)填写下表
| 各物质的溶液(杂质) |
除去杂质所需试剂 |
离子方程式 |
| Na2CO3(NaHCO3) |
||
| FeCl2(FeCl3) |
||
| Fe(Al) |
||
| SiO2(CaCO3) |