(10分)一定条件下,在体积为3 L的密闭容器中,一氧化碳与氢气反应生成甲醇(催化剂为Cu2O/ZnO):CO(g)+2H2(g) 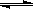 CH3OH(g)
CH3OH(g)
根据题意完成下列各题:
(1)反应达到平衡时,平衡常数表达式K= ,升高温度,K值 (填“增大”、“减小”或“不变”)。
(2)在500℃,从反应开始到平衡,氢气的平均反应速率v(H2)=
(3)在其他条件不变的情况下,对处于E点的体系体积压缩到原来的1/2,下列有关该体系的说法正确的是
a. 氢气的浓度减少 b. 正反应速率加快,逆反应速率也加快
c. 甲醇的物质的量增加 d. 重新平衡时n(H2)/n(CH3OH)增大
(4)据研 究,反应过程中起催化作用的为Cu2O,反应体系中含少量CO2有利于维持催化剂Cu2O的量不变,原因是: (用化学方程式表示)
究,反应过程中起催化作用的为Cu2O,反应体系中含少量CO2有利于维持催化剂Cu2O的量不变,原因是: (用化学方程式表示)
氢氧两种元素形成的常见物质有H2O与H2O2,在一定条件下均可分解。
(1)已知:
| 化学键 |
断开1mol化学键所需的能量(kJ) |
| H—H |
436 |
| O—H |
463 |
| O=O |
498 |
①H2O的电子式是。
②H2O(g)分解的热化学方程式是。
③11.2 L(标准状况)的H2完全燃烧,生成气态水,放出kJ的热量。
(2)某同学以H2O2分解为例,探究浓度与溶液酸碱性对反应速率的影响。常温下,按照如表所示的方案完成实验。
| 实验编号 |
反应物 |
催化剂 |
|
| a |
50 mL 5% H2O2溶液 |
1 mL 0.1 mol·L-1 FeCl3溶液 |
|
| b |
50 mL 5% H2O2溶液 |
少量浓盐酸 |
1 mL 0.1 mol·L-1 FeCl3溶液 |
| c |
50 mL 5% H2O2溶液 |
少量浓NaOH溶液 |
1 mL 0.1 mol·L-1 FeCl3溶液 |
| d |
50 mL 5% H2O2溶液 |
MnO2 |
①测得实验a、b、c中生成氧气的体积随时间变化的关系如图1所示。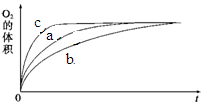
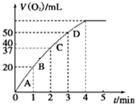
图1图2
由该图能够得出的实验结论是_________。
②测得实验d在标准状况下放出氧气的体积随时间变化的关系如图2所示。解释反应速率变化的原因:。
根据表中信息回答下列问题。
| 元素 |
Si |
P |
S |
Cl |
| 单质与氢气 反应的条件 |
高温 |
磷蒸气与氢气能反应 |
加热 |
光照或点燃时发生爆炸而化合 |
(1)S在元素周期表中的位置是。
(2)根据表中信息可知,Si、P、S、Cl 四种元素的的非金属性依次增强。用原子结构解释原因:同周期元素电子层数相同,从左至右,,原子半径逐渐减小,得电子能力逐渐增强。
(3)25℃时,以上四种元素的单质与氢气反应生成l mol气态氢化物的反应热如下:
a.+34.3 kJ·mol-1 b.+9.3 kJ·mol-1 c.−20.6 kJ·mol-1 d.−92.3 kJ·mol-1
请写出固态白磷(P4)与H2反应生成气态氢化物的热化学方程式。
(4)探究同主族元素性质的一些共同规律,是学习化学的重要方法之一。已知硒(Se)是人体必需的微量元素,其部分信息如图。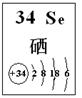
①下列有关说法正确的是(填字母)。
a. 原子半径:Se>S>P b. 稳定性:H2Se>H2S
c. 因为酸性H2Se<HCl,所以非金属性Se<Cl
d. SeO2是酸性氧化物,能与烧碱溶液反应
②在下表中列出对H2SeO3各种不同化学性质的推测,举例并写出相应的化学方程式。
| 编号 |
性质推测 |
化学方程式 |
| 1 |
氧化性 |
H2SeO3+4HI=Se↓+2I2+3H2O |
| 2 |
||
| 3 |
有一种细菌在酸性水溶液、氧气存在下,可以将黄铜矿(主要成分是CuFeS2,含少量杂质SiO2)氧化成硫酸盐。运用该原理生产铜和绿矾(FeSO4·7H2O)的流程如下: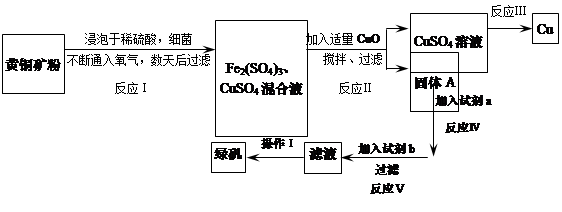
回答下列问题:
(1)已知:
| Fe2+ |
Cu2+ |
Fe3+ |
|
| 开始转化成氢氧化物沉淀时的pH |
7.6 |
4.7 |
2.7 |
| 完全转化成氢氧化物沉淀时的pH |
9.6 |
6.7 |
3.7 |
(1)加入CuO将溶液的pH调节到约为4,结合平衡移动原理解释该操作的原因。
(2)写出能实现反应Ⅲ的化学方程式。
(3)试剂b为。
(4)欲从滤液中获得绿矾晶体,操作Ⅰ应为浓缩、、。
(5)反应Ⅰ的化学方程式。
高纯硅生产流程如下: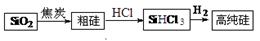
(1)由SiO2制粗硅的化学方程式是,该反应不能说明碳的非金属性强于硅,原因是,请写出一个能说明碳的非金属性强于硅的化学方程式。
(2)900℃以上,H2与SiHCl3发生反应:SiHCl3(g)+ H2(g) Si(s) + 3HCl(g) ΔH>0。将一定量的反应物通入固定容积的密闭容器中进行反应。下列说法正确的是(填字母)。
Si(s) + 3HCl(g) ΔH>0。将一定量的反应物通入固定容积的密闭容器中进行反应。下列说法正确的是(填字母)。
a.在恒温条件下,若容器内压强不变,则该反应一定达到化学平衡状态
b.增大SiHCl3的用量,可提高SiHCl3的平衡转化率
c.升高温度可加快反应速率,且提高硅的产率
(3)该流程中可以循环使用的物质是。
KMnO4是一种重要的氧化剂。
(1)①在酸性条件下KMnO4的氧化性会增强。用来酸化KMnO4溶液的最佳试剂是。
a.硝酸 b.硫酸 c.盐酸
②将 氧化C2O42−的离子方程式补充完整:
氧化C2O42−的离子方程式补充完整:
□MnO4−+□C2O42−+□==□Mn2+ +□CO2↑+□。
(2)某同学为了探究KMnO4溶液和Na2C2O4(草酸钠)溶液的反应过程,进行如下实验:
①配制100 mL 0.0400 mol·L-1的Na2C2O4溶液,除用到托盘天平、药匙、烧杯、量筒、玻璃棒等仪器外,还必须用到的玻璃仪器是。
②将KMnO4溶液逐滴滴入一定体积的酸性Na2C2O4溶液中(温度相同,并不断振荡),记录的现象如下:
| 滴入KMnO4溶液的次序 |
KMnO4溶液紫色褪去所需的时间 |
| 先滴入第1滴 |
60 s |
| 褪色后,再滴入第2滴 |
15 s |
| 褪色后,再滴入第3滴 |
3 s |
| 褪色后,再滴入第4滴 |
1 s |
请分析KMnO4溶液褪色时间变化的可能原因。
③用配制好的0.040 0 mol·L-1的Na2C2O4溶液来标定某KMnO4溶液的浓度。每次准确量取25.00 mLNa2C2O4溶液,然后用酸化后的KMnO4溶液滴定。滴定三次分别消耗的KMnO4溶液的体积是20.00 mL、19.80 mL、20.20 mL,则KMnO4溶液的浓度为。