下列离子方程式正确的是( )
| A.FeCl3溶液中滴加过量Na2S溶液:2Fe3++S2—═2Fe2++S↓ |
| B.将Na2O2固体投入H218O中:2Na2O2+2H218O=4Na++4OH-+18O2↑ |
| C.向NH4Al(SO4)2溶液中滴入Ba(OH)2溶液,恰好使SO42—完全沉淀: NH4++Al3++2SO42—+2Ba2++4OH—= Al(OH)3↓+NH3·H2O+2BaSO4↓[ |
| D.少量CO2通入苯酚钠溶液中:2C6H5O—+CO2+H2O = 2C6H5OH+CO32— |
将H2(g)和Br2(g)充入恒容密闭容器,恒温下发生反应
H2(g)+Br2(g) 2HBr(g) △H<0,平衡时Br2(g)的转化率为a;若初始条件相同,绝热下进行上述反应,平衡时Br2(g)的转化率为b。a与b的关系是( )
2HBr(g) △H<0,平衡时Br2(g)的转化率为a;若初始条件相同,绝热下进行上述反应,平衡时Br2(g)的转化率为b。a与b的关系是( )
| A.a>b | B.a=b | C.a<b | D.无法确定 |
一定条件下,在密闭容器里进行如下可逆反应:
|
S2Cl2(橙黄色液体)+Cl2(气) 2SCl2(鲜红色液体) △H =-61.16 kJ·mol-1下列说法正确的是( )
A.单位时间里生成n mol S2Cl2的同时也生成2n mol Cl2一定温度下,向a L密闭容器中加入2 mol NO2(g),发生反应:
2NO2 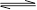 2NO+O2,此反应达到平衡状态时的标志是( )
2NO+O2,此反应达到平衡状态时的标志是( )
| A.混合气体的颜色变浅 |
| B.混合气体的密度不再变化 |
| C.混合气中NO2、NO、O2物质的量之比为2:2:1 |
| D.单位时间内生成2n mol NO,同时生成2n mol NO2 |
已知反应A2(g)+2B2(g)  2AB2(g) △H<0,下列说法正确的是( )
2AB2(g) △H<0,下列说法正确的是( )
| A.升高温度,正向反应速率增加,逆向反应速率减小 |
| B.升高温度有利于反应速率增加,从而缩短达到平衡的时间 |
| C.达到平衡后,升高温度或增大压强都有利于该反应平衡正向移动 |
| D.达到平衡后,降低温度或减小压强都有利于该反应平衡正向移动 |
一定温度下,在2 L的密闭容器中,X、Y、Z三种气体的物质的量随时 间变化的曲线如下图所示。下列描述正确的是( )
间变化的曲线如下图所示。下列描述正确的是( )
| A.反应开始到10 s,用Z表示的反应速 率为0.158 mol·(L·s)-1 |
| B.反应开始到10 s,X的物质的量浓度 减少了0.79 mol·L-1 |
| C.反应开始到10 s,Y的转化率为79.0% |
D.反应的化学方程式X(g)+Y(g)  z (g) z (g) |