
(1)已知某温度下,反应2SO2+O2 2SO3,的平衡常数K=19,在该温度下的体积
2SO3,的平衡常数K=19,在该温度下的体积 固定的密闭容器中充
固定的密闭容器中充 入C(SO2)=1mol·L-1,C(O2)="1" mol·L-1,当反应在该温度下SO2转化率
入C(SO2)=1mol·L-1,C(O2)="1" mol·L-1,当反应在该温度下SO2转化率 为80%时,该反应
为80%时,该反应
(填“是”或“否”)达到化学平衡状态,若未达到,向  (填“正反应”或“逆反应”) 方向进行。
(填“正反应”或“逆反应”) 方向进行。
(2)对于可逆反应:aA(g) +bB(g)  cC(g)+dD(g) △H = a kJ·mol
cC(g)+dD(g) △H = a kJ·mol -1;
-1;
若增大压强平衡向正反应方向移动,则a+b c+d(填“>”或“<”);若升高温度,平衡向正反应方向移动,则a_______0(填“>”或“<”)
常温下,将amol N2与bmol H2的混合气体通入一个固定容积的密闭容器中,发生如下反应:N2(g)+3H2(g)2NH3(g)。
(1)若反应进行到某时刻t时,nt(N2)=13mol,nt(NH3)=6mol,则a的值为________。
(2)反应达到平衡时,混合气体的体积为716.8 L(标准状况下),其中NH3的体积分数为25%,计算平衡时NH3的物质的量为_____。
(3)原混合气体与平衡混合气体的总物质的量之比(写最简整数化,下同)n始∶n平=________。
(4)原气体中a∶b=________。
(5)达到平衡时混合气体中,n(N2)∶n(H2)∶n(NH3)=________。
在2 L密闭容器中,800℃时反应2NO(g)+O2(g) 2NO2(g)体系中,n(NO)随时间的变化如表:
2NO2(g)体系中,n(NO)随时间的变化如表:
| 时间/s |
0 |
1 |
2 |
3 |
4 |
5 |
| n(NO)/mol |
0.020 |
0.010 |
0.008 |
0.007 |
0.007 |
0.007 |
(1)上述反应________(填“是”或“不是”)可逆反应。
(2)如图所示,表示NO2变化曲线的是______。用O2表示从0~2s内该反应的平均速率v=________。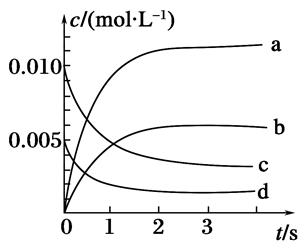
(3)能说明该反应已达到平衡状态的是________(填序号)。
a.v(NO2)=2v(O2)
b.容器内压强保持不变
c.v逆(NO)=2v正(O2)
d.容器内密度保持不变
在某一容积为5 L的密闭容器内,加入0.2mol 的CO和0.2mol的H2O(g),在催化剂存在的条件下高温加热,发生如下反应:CO(g)+H2O(g) CO2(g)+H2(g),反应放出热量。反应中CO2的浓度随时间变化的情况如下图所示。
CO2(g)+H2(g),反应放出热量。反应中CO2的浓度随时间变化的情况如下图所示。
(1)根据图中数据,从反应开始至达到平衡时,CO的化学反应速率为________;反应平衡时c(H2)=________。
(2)判断该反应达到平衡的依据是________(填序号)。
| A.CO减少的化学反应速率和CO2减少的化学反应速率相等 |
| B.CO、H2O、CO2、H2的浓度都相等 |
| C.CO、H2O、CO2、H2的浓度都不再发生变化 |
| D.正、逆反应速率都为零 |
用纯净的碳酸钙和稀盐酸反应制取二氧化碳气体,请回答:
(1)实验过程如图所示,分析判断:__________段化学反应速率最快,________段收集的二氧化碳气体最多。
(2)为了减缓上述反应的化学速率,欲向溶液中加入下列物质,你认为可行的是________(填字母编号)。
| A.蒸馏水 | B.NaCl固体 | C.NaCl溶液 | D.浓盐酸 |
(3)除了上述方法外,你认为还可以采取哪些措施来减缓化学反应速率?(至少回答两种)_______________________________________________________________。
将等物质的量的A、B混合于2 L的密闭容器中,发生如下反应:3A(g)+B(g) xC(g)+2D(g),经5min后,测得D的浓度为0.5mol/L,c(A)∶c(B)=3∶5,C的平均反应速率为0.1mol/(L·min)。求:
xC(g)+2D(g),经5min后,测得D的浓度为0.5mol/L,c(A)∶c(B)=3∶5,C的平均反应速率为0.1mol/(L·min)。求:
(1)此时A的浓度c(A)=________mol/L,反应开始前容器中的A、B的物质的量:n(A)=n(B)=________mol。
(2)B的平均反应速率:v(B)=________mol/(L·min)。
(3)x的值为________。