已知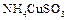 与足量的10 mol/L硫酸混合微热,产生下列现象: ①有红色金属生成 ②产生刺激性气味的气体 ③溶液呈现蓝色 据此判断下列说法正确的是( )
与足量的10 mol/L硫酸混合微热,产生下列现象: ①有红色金属生成 ②产生刺激性气味的气体 ③溶液呈现蓝色 据此判断下列说法正确的是( )
| A.反应中硫酸作氧化剂 |
B.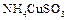 中硫元素被氧化 中硫元素被氧化 |
| C.刺激性气味的气体是氨气 |
D.1 mol 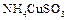 完全反应转移0.5 mol电子 完全反应转移0.5 mol电子 |
当光束通过淀粉溶液时,可观察到丁达尔效应,表明淀粉溶液是
| A.胶体 | B.溶液 | C.悬浊液 | D.乳浊液 |
美籍华裔科学家钱永键等三位科学家因在发现和研究各种绿色荧光蛋白方面做出杰出贡献而获得2008年诺贝尔化学奖。绿色荧光蛋白属于
| A.单质 | B.有机物 | C.氧化物 | D.无机物 |
被大气中存在的酸性气体污染,pH值小于5.65的降水叫酸雨。下列因素会造成酸雨的是
| A.燃烧脱硫处理的煤 | B.机动车辆排放尾气 |
| C.垃圾分类回收利用 | D.使用氢氧燃料电池 |
下列实验操作中错误的是
| A.分液时,分液漏斗下层液体从下口放出,上层液体也从下口倒出 |
| B.蒸馏时,应使温度计水银球靠近蒸馏烧瓶支管口 |
| C.蒸发结晶时应将溶液直接蒸干 |
| D.称量非腐蚀性药品应放在称量纸上置于托盘天平的左盘,砝码放在托盘天平的右 |
盘中
有甲、乙、丙、丁四种金属,把甲、丙浸入稀硫酸中,用导线连接时丙为负极;把乙、丁分别浸入稀硫酸中,丁产生气泡的速率更大;把甲、乙用导线连接浸入稀硫酸中,甲上有气泡冒出;把丙浸入丁的硝酸盐溶液中,丙的表面有丁析出。这四种金属的活动性由强到弱的顺序是
| A.甲>乙>丙>丁 | B.丙>丁>乙>甲 |
| C.丙>丁>甲>乙 | D.丁>乙>甲>丙 |