在一固定容积的密闭容器中,保持一定条件下进行以下反应:X(g)+2Y(g)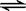 3Z(g),已知加入2 molX和3molY。达到平衡后,生成a mol Z。
3Z(g),已知加入2 molX和3molY。达到平衡后,生成a mol Z。
(1)在相同实验条件下,若在同一容器中改为加入4 mol X和6 mol Y,达到平衡后,Z的物质的量为
mol。
(2)在相同实验条件下,若在同一容器中改为加入3 mol X和2 mol Y,若要求在反应混合气体中Z体积分数不变,则还需加入Z mol。
(3)在相同实验条件下,若在同一容器中改为加入0.5molX,则需加入 mol Y,
mol Z,才能使平衡时Z为0.6a mol。
下列各物质的转化关系如下图所示,其中A是一种高熔点固体,D是一种棕红色固体。
回答下列问题:
⑴C的化学式为;J的化学式为。
⑵写出由A生成H的离子反应方程式:。
⑶写出图中由F转化为G反应的离子方程式:。
下图为氢氧燃料电池的示意图:
⑴若以稀硫酸为电解液,则a极为____极。
⑵若以KOH溶液作电解液,则b极上的电极反应式为_______________________,放电一段时间后电解液的pH将________(填“变大”、“变小”或“不变”)。
25℃时,1L 0.01mol/LHCl溶液,水的离子积常数Kw为,溶液中H+的物质的量浓度为,水电离出的H+的物质的量浓度为,向上述溶液中加入1L 0.008mol/L的NaOH溶液,反应后溶液的pH为。
(10分)某离子晶体晶胞的结构如图所示。X(·)位于立方体顶点,Y(o)位于立方体中心。试分析:
(1)晶体中每个Y同时吸引着________个X,每个X同时吸引着________个Y,该晶体的化学式为________。
(2)晶体中每个X周围与它最接近且距离相等的X共有________个。
(3)晶体中距离最近的2个X与1个Y形成的夹角∠XYX是________。
(4)设该晶体的摩尔质量为Mg/mol,晶体密度为ρg/cm3,阿伏加德罗常数的值为NA,则晶体中两个距离最近的X中心距离为________cm。
根据下列某些短周期元素中元素性质的有关信息,回答下列问题:
| ① |
② |
③ |
④ |
⑤ |
⑥ |
⑦ |
⑧ |
⑨ |
⑩ |
|
| 原子半径 /10-10m |
0.37 |
1.86 |
0.74 |
1.43 |
0.77 |
1.10 |
0.99 |
1.52 |
0.75 |
0.71 |
| 最高价态 |
+1 |
+1 |
+3 |
+4 |
+5 |
+7 |
+1 |
+5 |
||
| 最低价态 |
-1 |
-2 |
-4 |
-3 |
-1 |
-3 |
-1 |
(1)元素①②⑧的第一电离能由大到小的顺序是 ;元素③⑥⑨的电负性由大到小的顺序是 (以上均用元素符号填空)。
(2)元素⑤⑥⑦中的某两种形成的化合物中,每个原子都满足最外层为8电子稳定结构的物质有 (写化学式)。
(3)某元素R 的原子半径为1.02×10-10m,它与钠形成Na2R2,若物质Na2R2是一种含有非极性共价键的离子化合物,其电子式是 (R用元素符号表示)。
(4)元素①和⑨形成阳离子,其结构式为 ,其中心原子以 杂化轨道成键。
(5)元素⑤的原子基态电子排布式为 。