乙炔是有机合成工业的一种原料。工业上曾用CaC2与水反应生成乙块。
⑴CaC2中C22-与O22+互为等电子体,O22+的电子式可表示为 ;1mol O22+中含有的 键数目为 。
键数目为 。
⑵将乙炔通入[Cu(NH3)2]Cl溶液生成CaC2红棕色沉淀。Cu+基态核外电子排布式为 。
⑶乙炔与氢氰酸反应可得丙烯腈(H2C=CH-C N)。丙烯腈分子中碳原子轨道杂化类型是 ;分子中处于同一直线上的原子数目最多为 。
N)。丙烯腈分子中碳原子轨道杂化类型是 ;分子中处于同一直线上的原子数目最多为 。
⑷CaC2晶体的晶胞结构与NaCl晶体的相似(如图所示),但CaC2晶体中哑铃形C22-的存在,使晶胞沿一个方向拉长。CaC2晶体中1个Ca2+周围距离最近的C22-数目为 。
已知氮元素有许多化合价,其化合价有-3、0、+1、+2、+3、+4、+5
(1)下表是硝酸与某种金属M在某些条件下反应所得还原产物的关系:
通过分析上表可得出的结论是:当硝酸与金属M反应时,________________。
金属锌与某浓度的硝酸反应时,无气体产生,则此化学反应中被还原的硝酸与参加反应的硝酸物质的量之比是________。
(2)以氨作为燃料的固体氧化物(含有O2-)燃料电池,具有全固态结构、能量效率高、无污染等特点,另外氨气含氢量高,不含碳,易液化,方便运输和贮存,是很好的氢源载体。其工作原理如图所示:
①该电池工作时的总反应为______ __
②固体氧化物作为电池工作的电解质,O2-移动方向为________(选填“由电极a向电极b”或“由电极b向电极a”)。
③该电池工作时,在接触面上发生的电极反应为________。
(3)N2O5是一种新型硝化剂,其性质和制备 受到人们的关注。如图所示装置可用于制备N2O5,写出在电解池中生成N2O5的电极反应式________________。
在锌湿法冶炼过程中,会产生大量铜镉渣(主要含有Zn、Cd、Fe、Cu等),直接丢弃会造成环境污染,也是资源浪费,以下为回收处理铜镉渣制备硫酸锌晶体的工业流程:
已知:硫酸锌晶体易溶于水,难溶于酒精。
(1)加入硫酸的目的。
(2)硫酸不能溶出铜,加入锰粉是为了结合铁离子的变价来传递电子,将铜溶出,锰粉的主要成分为MnO2,相关方程式为2Fe3++Cu=2Fe2++Cu2+和。
(3)由硫酸锌溶液获得硫酸锌晶体,必要的操作方法为。
(4)制得的硫酸锌晶体需要洗涤,选择的试剂为,原因是。
下表为元素周期表的一部分,请参照元素①-⑨在表中的位置,
回答下列问题:
| 族 周期 |
IA |
0 |
||||||
| 1 |
① |
ⅡA |
ⅢA |
ⅣA |
ⅤA |
ⅥA |
ⅦA |
|
| 2 |
② |
③ |
④ |
|||||
| 3 |
⑤ |
⑨ |
⑥ |
⑦ |
⑧ |
(1)由①、②两种元素组成的相对分子质量为28的有机物的空间构型是,
该物质与溴水发生加成反应的化学方程式是。
(2)用电子式表示④的简单氢化物的形成过程如下:;
(3) 请设计实验比较元素⑥与⑨金属性的相对强弱:_;
(4) 用①元素的单质与④元素的单质可以制成电池,电池中装有KOH浓溶液,将多孔的惰性电极甲和乙浸入KOH溶液中,在甲极通入①的单质,乙极通入④的单质,则甲极的电极反应式为:。
(5)由表中①、③、④、⑥、⑧元素形成的常见物质X、Y、Z、M、N可发生以下反应: 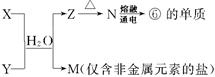
X溶液与Y溶液反应的离子方程式为,工业上常用单质⑥冶炼难熔的金属,写出氧化铁和单质⑥在高温下反应的化学方程式。
Ⅰ.下面列出了几组物质或粒子,请将合适的组号填写在空格上。
①金刚石与“足球烯”(C60);②D与T;③16O、17O和18O;④氧气(O2)与臭氧(O3);⑤乙醇(CH3CH2OH)和甲醚(CH3OCH3);
(1)是同素异形体的, (2)是同位素的,(3)是同分异构体的。
Ⅱ.在下列变化中:①干冰气化 ②硝酸钾熔化 ③食盐溶于水 ④HCl溶于水 ⑤蔗糖溶于水 ⑥HI分解。用序号填空:(1)未破坏化学键的是,(2)仅离子键被破坏的是,
(3)仅共价键被破坏的是。
从海水制备金属镁的流程如图所示: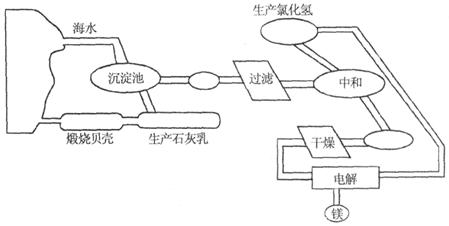
(1)为了节约成本,充分利用海滩资源,用贝壳经过一系列反应可以制得石灰乳,请写出有关反应的化学方程式:__________;__________。
(2)向石灰乳中加入MgCl 溶液,充分搅拌、过滤、洗涤。写出该反应的化学方程式:__________。
溶液,充分搅拌、过滤、洗涤。写出该反应的化学方程式:__________。
(3)从熔点与硬度方面来看,镁合金与镁相比较,其特点有__________。