根据下列框图回答问题(答题时,方程式中的M、E用所对应的元素符号表示):
(1)写出M溶于稀硫酸和H2O2混合液的化学方程式: 。
(2)写出X→Y的离子方程式: 。
(3)写出Cl2将Z氧化为K2EO4的化学方程式: 。
②K2EO4是一种新型的自来水处理剂,它的性质和作用是 。
| A.有强氧化性,可消毒杀菌,还原产物能吸附水中杂质 |
| B.有强还原性,可消毒杀菌,氧化产物能吸附水中杂质 |
| C.有强氧化性,能吸附水中杂质,还原产物能消毒杀菌 |
| D.有强还原性,能吸附水中杂质,氧化产物能消毒杀菌 |
Ⅰ、有下列五种烃:① ②
②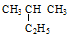 ③乙烷 ④戊烷 ⑤
③乙烷 ④戊烷 ⑤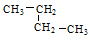 ,其中互为同分异构体的是(填序号),②与⑤之间的关系为,
,其中互为同分异构体的是(填序号),②与⑤之间的关系为,
②③④⑤四种物质按它们的沸点由高到低的顺序排列正确的是(填序号)
Ⅱ、某烃A是有机化学工业的基本原料,其产量可以用来衡量一个国家的石油化工发展水平,A在一定条件下可发生如图所示的转化,请回答下列问题: 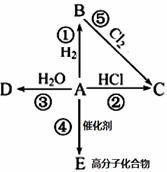
(1)写出A的电子式,E的结构简式为
(2)写出下列反应化学方程式,并注明③⑤反应类型
② _____________________________________________
③ _____________________ ,反应类型________;
⑤ _____________________ ,反应类型________;
(3)除去B中混有的少量杂质A,所用的试剂为
正丁醚常用作有机反应的溶剂。实验室制备正丁醚的主要实验装置如下图:
反应物和产物的相关数据如下
合成正丁醚的步骤:
①将6 mL浓硫酸和37 g正丁醇,按一定顺序添加到A中,并加几粒沸石。
②加热A中反应液,迅速升温至135℃,维持反应一段时间。分离提纯:
③待A中液体冷却后将其缓慢倒入盛有70 mL水的分液漏斗中,振摇后静置,分液得粗产物。
④粗产物依次用40 mL水、20 mL NaOH溶液和40 mL水洗涤,分液后加入约3 g无水氯化钙颗粒,静置一段时间后弃去氯化钙。
⑤将上述处理过的粗产物进行蒸馏,收集馏分,得纯净正丁醚11 g。
请回答:
(1)步骤①中浓硫酸和正丁醇的添加顺序为______________________________。
写出步骤②中制备正丁醚的化学方程式______________________________。
(2)加热A前,需先从__________(填“a”或“b”)口向B中通入水。
(3)步骤③的目的是初步洗去,振摇后静置,粗产物应从分液漏斗的(填“上”或“下”)口分离出。
(4)步骤④中最后一次水洗的目的为______________________________。
(5)步骤⑤中,加热蒸馏时应收集__________(填选项字母)左右的馏分。
a.100℃ b. 117℃ c. 135℃ d.142℃
(6)反应过程中会观察到分水器中收集到液体物质,且分为上下两层,随着反应的进行,分水器中液体逐渐增多至充满时,上层液体会从左侧支管自动流回A。分水器中上层液体的主要成分为__________,下层液体的主要成分为__________。(填物质名称)
(7)本实验中,正丁醚的产率为__________。
化学家利用钯(Pd)作催化剂,将有机化合物进行“裁剪”“缝合”,创造出具有特殊功能的新物质而荣获2010年诺贝尔化学奖。赫克反应(Heck反应)的通式可表示为:
(R—X中的R通常是不饱和烃基或苯环;R′CH=CH2通常是丙烯酸酯或丙烯腈CH2=CH—CN等):
现有A、B、C、D等有机化合物有如下转化关系(部分反应条件省略)
请回答下列问题:
(1)反应Ⅰ的化学方程式为__________________________________________________。
(2)已知腈基(—C≡N)也具有不饱和性(可催化加氢),写出CH2=CH—CN完全催化加氢的化学方程式:________________________________________。写出上述催化加氢后的产物的同分异构体的结构简式________________________________________。
(3)丙烯腈(CH2=CH—CN)可发生加聚反应生成一种高聚物,此高聚物的结构简式为______________________________。
(4)写出B转化为C的化学方程式:______________________________反应类型为__________。
(5)D的结构简式为(必须表示出分子的空间构型)______________________________。
图中A~G均为有机化合物,根据图中的转化关系(反应条件略去),回答下列问题:
(1)环状化合物A的相对分子质量为82,其中含碳87.80%,含氢12.2%。B的一氯代物仅有一种,B的结构简式为______________________________。
(2)M是B的一种同分异构体,M能使溴的四氯化碳溶液褪色,分子中所有的碳原子共平面,则M的结构简式为______________________________。
(3)写出由C生成D的化学方程式______________________________反应类型是__________,由G生成A的化学方程式______________________________反应类型是__________。由G生成F的化学方程式______________________________反应类型是__________。G发生催化氧化的化学方程式______________________________。
(4)F的核磁共振氢谱图有__________个吸收峰,峰面积之比为__________。
(1)一定条件下某烃与H2按物质的量之比1:2加成生成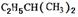 ,则该烃的结构简式为______________________________;
,则该烃的结构简式为______________________________;
(2)某有机物X分子中只含C、H、O三种元素,相对分子质量小于110,其中氧元素的质量分数为14.8%,已知该物质可与FeCl3溶液发生显色反应,则X的分子式为__________。
若1 mol X与浓溴水反应时消耗了3 mol Br2,则X的结构简式为____________________。
(3)分子式为C4H8的烃,核磁共振氢谱图中有两个吸收峰,峰面积比为3:1,请写出符合条件的所有物质的结构简式
(4)下列括号内为杂质,将除去下列各组混合物中杂质所需的试剂和方法填写在横线上。
① 溴乙烷(乙醇)____________________________________________________________
② 苯酚(苯)______________________________________________________________________
写出②操作中涉及到的反应的化学方程式________________________________________
(5)已知: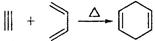 ,如果要合成
,如果要合成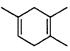 所用的原始原料可以是()
所用的原始原料可以是()
A.2-甲基-l,3-丁二烯和2-丁炔 B.2,3-二甲基-1,3-戊二烯和乙炔
C.2,3-二甲基-l,3-丁二烯和丙炔 D.1,3-戊二烯和2-丁炔