阅读下列两段材料,请回答下列问题:
材料一:2006年全国理综I第9题:把分别盛有熔融的氯化钾、氯化镁、氯化铝的三个电解槽串联,在一定条件下通电一段时间后,析出钾、镁、铝的物质的量之比为 ( )
( )
| A.1:2:3 | B.3:2:l | C.6:3:1 | D.6:3:2 |
材料二:已知下列表中有关物质的熔、沸点如下:
| 物质 |
K2O |
MgO |
Al2O3 |
KCl |
MgCl2 |
AlCl3 |
| 熔点(℃) |
881 |
2852 |
2015 |
711 |
714 |
190(259KPa) |
| 沸点(℃) |
-- |
3600 |
2980 |
1437 |
1412 |
181 |
(1)有人认为材料一中的题干与选项有矛盾,若选项正确,则结 合材料二可推知氯化钾、氯化镁、氯化铝三种物质中有一种物质是不符合题意的,这种物质是 ,其理由是
合材料二可推知氯化钾、氯化镁、氯化铝三种物质中有一种物质是不符合题意的,这种物质是 ,其理由是
。
(2)有人认为材料一中的题干正确,只要把一个正确的选项补加进去就是一道好题,你认为选项改加“(I)0:0:0”和“(II)6:3: 0”哪个好? (填写编号)
(3)也有人认为只要把氯化钾、氯化镁、氯化铝中的其中一种物质改为材料二表格中另一种物质也符合题意。写出电解这种物质的化学方程式:
下表是A、B两种有机物的有关信息: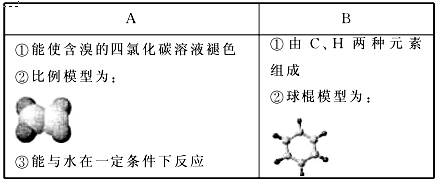
 根据表中信息回答下列问题:
根据表中信息回答下列问题:
(1)A与含溴的四氯化碳溶液反应的生成物的名称为________________;
写出在一定条件下,A与水反应的化学反应方程式___________。
(2)A的同系物用通式Cn Hm表示,B的同系物用通式Cx Hy表示,当A、B同系物分别出现同分异构体时,碳原子数最小值n =________,x =________。
(3)B具有的性质是______________(填序号)。
①无色无味液体;②有毒;③不溶于水;④密度比水大; ⑤与酸性KMnO4溶液和溴水反应使之褪色;⑥任何条件下不与氢气反应;⑦使溴水颜色变浅或褪色
为了测定某有机物A的结构,做如下实验:①将2.3 g该有机物完全燃烧,生成0.1 mol CO2和2.7 g水;②用质谱仪测定其相对分子质量,得如图一所示的质谱图;③用核磁共振仪处理该化合物,得到如图二所示图谱,图中三个峰的面积之比是1:2:3。试回答下列问题:
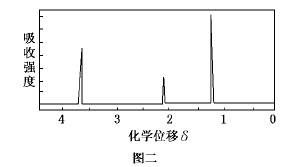
(1)有机物A的相对分子质量是________。
(2)有机物A的实验式是________。
(3)能否根据A的实验式确定A的分子式________(填“能”或“不能”),若能,则A的分子式是________(若不能,则此空不填)。
(4)写出有机物A可能的结构简式________。
如图是由4个碳原子结合成的五种有机物(氢原子没有画出)
(1)写出有机物(a)的系统命名法的名称________。
(2)有机物(a)有一种同分异构体,试写出其结构简式____________。
(3)上述有机物中与(c)互为同分异构体的是________(填代号)。
(4)任写一种与(e)互为同系物的有机物的结构简式______ __________。
__________。
(5)上述有机物中不能与溴水反应使其褪色的有________(填代号)。
(6)(a)(b)(c)(d)(e)五种物质中,4个碳原子一定处于同一平面的有
(填代号)。
(7分)在KClO3+6 H Cl(浓)=KCl+3Cl2↑+3H2O的反应中,氧化剂是___________,还原产物是_________,得电子与失电子个数比是____________,氧化产物与还原产物的质量比是________,反应中被氧化的盐酸和未被氧化盐酸的质量比是,
试用双线桥法表示上述氧化还原反应_________________________
(13分)有A、B、C、D四种化合物,分别由K+、Ba2+、SO42-、CO32-、OH-中的两种组成,它们具有下列性质:①A不溶于水和盐酸;②B不溶于水,但溶于盐酸,并放出无色无刺激性气味的气体E;③C的水溶液呈碱性,与硫酸反应生成A;④D可溶于水,与硫酸作用时放出气体E,E可使澄清石灰水变浑浊。
(1)推断A、B、C、D、E的化学式。
A;B;C;D;E;
(2)写出下列反应的离子方程式。
B与盐酸反应
C与硫酸反应
D与硫酸反应
E与澄清石灰水反应