接触法制硫酸工艺中,其主反应在450℃并有催化剂存在下进行:
2SO2(g)+O2(g) 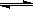 2SO3(g) △H=-190 kJ·mo1-1
2SO3(g) △H=-190 kJ·mo1-1
(1)在一个固定容积为5L的密闭容器中充入0.20 mol SO2和0.10molO2,半分钟后达到平衡,测得容器中含SO30.18mol,则v(O2)=______mol·L-1·min-1
(2)下列条件的改变能加快其反应速率的是 (选填序号)
①升高温度
②保持体积不变,只增加氧气的质量
③保持体积不变,充入Ne使体系压强增大
④保持压强不变,充入Ne使容器的体积增大
(3)下列描述中能说明上述(1)反应已达平衡的是 (选填序号)
①v(O2)正=2v(SO3)逆
②SO2、O2、SO3的浓度之比为2:1:2
③单位时间内生成2n molSO2的同时生成2n mol SO3
④容器中气体的平均分子量不随时间而变化
⑤容器中气体的密度不随时间而变化
⑥容器中气体压强不随时间而变化
(4)在相同条件下发生上述反应,若要得到380kJ热量,则加入各物质的物质的量可能
是 。
| A.4 mo1SO2和2mol O2 | B.6mol SO2和6mo1 O2 |
| C.4mol SO2和4 mo1 O2 | D.6mo1 SO2和4 mo1 O2 |
在一定温度下的定容密闭容器中,当物质的下列物理量不再变化时,表明反应:A(s)+2B(g) C(g)+D(g)已达平衡的是___________________________。
C(g)+D(g)已达平衡的是___________________________。
①混合气体的压强②混合气体的密度③B的物质的量浓度④气体的总物质的量
在一个恒温恒容的密闭容器中,发生如下反应:CO(g)+H2O(g)CO2(g)+H2(g),开始时充入容器中的起始物质是:①0.1 mol CO,0.1 mol H2②0.1 mol CO,0.2 mol H2O③0.1 mol CO,0.1 mol H2O④0.1 mol CO,0.1 mol H2O,0.1 mol H2。达到平衡时容器中H2的物质的量由小到大的排列顺序是____________。
在一密闭容器中充入1 mol NO2,建立如下平衡:2NO2 N2O4。平衡时测得NO2的转化率为a%。其他条件不变,再充入1 mol NO2,待新平衡建立时,测得NO2的转化率为b%。则a和b的大小关系为________________。
N2O4。平衡时测得NO2的转化率为a%。其他条件不变,再充入1 mol NO2,待新平衡建立时,测得NO2的转化率为b%。则a和b的大小关系为________________。
下列各组反应哪几组是可逆反应?为什么?
(1)2H2+O2 2H2O与2H2O
2H2O与2H2O 2H2↑+O2↑
2H2↑+O2↑
(2)NH3+H2O====NH3·H2O与NH3·H2O==== +OH-
+OH-
(3)CaCO3(s)====CaCO3(aq)与CaCO3(aq)====CaCO3(s)
(4) +OH-====NH3·H2O与NH3·H2O====
+OH-====NH3·H2O与NH3·H2O==== +OH-
+OH-
(5)2NH3 3H2+N2与N2+3H2
3H2+N2与N2+3H2 2NH3
2NH3
(6)SO2+H2O====H2SO3与H2SO3====SO2+H2O
(7)2SO2+O2 2SO3与2SO3
2SO3与2SO3 2SO2+O2
2SO2+O2
(8)2HI H2↑+I2↑与H2+I2
H2↑+I2↑与H2+I2 2HI
2HI
已知T K和P kPa时,在容积为V L的密闭容器中充有1 mol A和1 mol B,保持恒温恒压,使反应: A(g)+B(g) C(g)达到平衡时, C的体积分数为40%。试完成下列有关问题:
C(g)达到平衡时, C的体积分数为40%。试完成下列有关问题:
(1)若使温度和压强在上述条件下恒定不变,在密闭容器中充入2 mol A和2 mol B,则反应达到平衡时,容器的体积为________,C的体积分数为________。
(2)若另选一容积固定不变的密闭容器,仍然控制温度为T K,使1 mol A和1 mol B反应达到平衡状态时, C的体积分数仍然为40%,则该密闭容器的体积为________。