下列平衡体系在体积不变时加入所给物质,平衡移动的是( )
A.FeCl3(aq)+3KSCN(aq)  Fe(SCN)3(aq)+3KCl(aq),加入KCl晶体 Fe(SCN)3(aq)+3KCl(aq),加入KCl晶体 |
B.N2(g)+3H2(g)  2NH3(g),加入HCl 2NH3(g),加入HCl |
C.CaCO3(s) CaO(s)+CO2(g),加入CaCO3 CaO(s)+CO2(g),加入CaCO3 |
D.2SO2(g)+O2(g) 2SO3(g),加入N2 2SO3(g),加入N2 |
用一带静电的玻璃棒靠近A、B两种纯液体流,根据图分析,这两种液体分子的极性正确的是( )。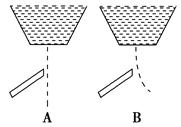
A.A是极性分子,B是非极性分子
B.A是非极性分子,B是极性分子
C.A和B都是极性分子
D.A和B都是非极性分子
CO2、CH4、BF3都是非极性分子,HF、H2O、NH3都是极性分子,由此推测ABn型分子是非极性分子的经验规律正确的是( )。
| A.所有原子在同一平面 |
| B.分子中每个键的键长应相等 |
| C.在ABn中A原子没有孤对电子 |
| D.A的相对原子质量小于B |
下列各组物质中,都是由极性键构成的极性分子的一组是( )。
| A.CH4 Br2 | B.H2O NH3 |
| C.CCl4 H2S | D.CO2 HCl |
具有手性碳原子的物质往往具有旋光性,存在对映异构体,下列化合物中存在对映异构体的是( )。
| A.C2H5CH=CHCH(CH3)—CH=CHC2H5 |
| B.2甲基丁烷 |
| C.甲酸 |
| D.C6H5CH(CH3)CHO |
下列物质的分子中,不具有对称性的是( )。
| A.CH3Cl | B.CH2Cl2 | C.CH2ClBr | D. |