现有三种物质A、B、C,它们均溶于水。其中有一种是酸,一种是碱,一种是盐,溶于水后电离,可以产生下表中的离子:
| 阳离子 |
Na+ H+ Ba2+ |
| 阴离子 |
OH- CO SO SO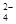 |
为鉴别它们,分别完成以下实验,其结果如下:
① A溶液与B溶液反应生成无色气体X,气体X可以和C溶液反应生成沉淀E,沉淀E可与B溶液反应;
② B溶液与C溶液反应生成白色沉淀D,沉淀D不溶于稀硝 酸。
酸。
请根据上述实验结果,填空:
(1)写出下列物质的化学式:X
(2)B溶于水后的电离方程式为
(3)鉴别B中阴离子的实验操作方法是
(4)B与C反应的离子方程式:
(16分)给出下列氧化还原反应,试回答下列问题。
(1) KMnO4+ KI+ H2SO4K2SO4+ MnSO4 + I2十 H2O
配平化学反应方程式
被还原的元素 ,发生氧化反应的物质。 (2) 3Cl2+ 6NaOH 5NaCl + NaClO3+ 3H2O
(2) 3Cl2+ 6NaOH 5NaCl + NaClO3+ 3H2O
用双线桥标出电子转移的方向和数目
氧化剂与还原剂的物质的量之比为,氧化产物是。
(3)11P+15CuSO4+24H2O=6H3PO4+15H2SO4+5Cu3P(反应中Cu3P中的P为负三价)。
该反应中Cu2+表现性(填氧化或还原);11molP中被P氧化的P是mol
(共9分)
(1)0.5 mol H2O的质量为 g,其中含有个水分子,共有个原子。
(2)质量都是50 g的 HCl、NH3、CO2、O2四种气体中,含有分子数目最少的是 _ ,在相同温度和相同压强条件下,体积最大的是,体积最小的是。
(3)配制50 mL 0.2 mol/L CuSO4溶液,需要CuSO4g;需要CuSO4·5H2O _g。
(4)中和相同体积、相同物质的量浓度的NaOH溶液,并使其生成正盐,需要相同物质的量浓度的HCl、H2SO4、H3PO4溶液的体积比为。
(共5分)用于提纯或分离物质的方法有:
| A.萃取分液 | B.加热分解 | C.蒸发结晶 | D.分液 E、蒸馏 F、过滤、G渗析等,请将提纯或分离的序号填在后面横线上。 |
(1)分离饱和食盐水与泥沙的混合物 _____
_____
(2)分离水和汽油的混合物 _____
(3)海水淡化 ______
(4)从碘水里提取碘 ______
(5)除去氢氧化铁胶体中混有的氯离子、钠离子 ______
______
(共6分) 现有①二氧化硫②蔗糖(C12H22O11)③纯碱 ④铜 ⑤碘的酒精溶液⑥液溴 ⑦石墨 ⑧熟石灰⑨硫酸铝溶液⑩烧碱十种物质,若根据物质的组成或性质进行分类,则(填对应的编号) 下列各组物质中:
⑴属于“混合物”的是_______________⑵能“导电”的是_________
⑶属于“非金属单质”的是___________⑷属于“电解质”的是___________
⑸属于“非电解质”的是⑹属于“碱类物质”的是
根据图示填空
(1)化合物A中含氧官能团的名称是。
(2)1mol A与2 mol H2反应生成1 mol E,其反应方程式是
___________________________________________________。
(3)B在酸性条件下与Br2反应得到D,D的结构简式是 。写出D与NaOH溶液反应的化学方程式_________________________________________。
。写出D与NaOH溶液反应的化学方程式_________________________________________。
(4)F的结构简式是。