下图中每一方框中的字母代表一种反应物或生成物(部分产物未列出):
已知C是紫红色金属固体,B的浓溶液和稀溶液都是有强氧化性。
(1)A的化学式是 ,E化学式是 ;
(2)电解反应的化学(或离子)方程式是 ;
(3)对200ml 1mol/L的A溶液进行电解,当有0.02mol电子发生转移时,溶液的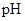 为
为
(假设溶液体积不变)。
现有四种试剂:①新制Cu(OH)2悬浊液;②浓硝酸;③AgNO3溶液;④碘水。
为了鉴别下列四瓶无色溶液,请你选择合适的试剂,将其序号填入相应的括号中。
(1)葡萄糖溶液(2)食盐溶液
(3)淀粉溶液(4)鸡蛋清溶液
(6 分)课本“交流•研讨”栏目有这样一组数据:破坏1mol氢气中的化学键需要吸收436kJ能量;破坏1/2mol 氧气中的化学键需要吸收249kJ的能量;形成水分子中1 molH—O键能够释放463kJ 能量。
下图表示氢气和氧气反应过程中能量的变化,请将图中①、②、③的能量变化的数值,填在下边的横线上。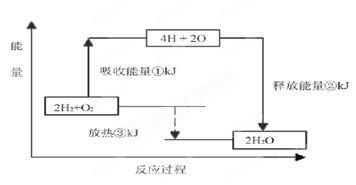
①_______________ kJ ②________________ kJ ③_________________kJ
(1)20世纪30年代,Eyring和Pzer在碰撞理论的基础上提出化学反应的过渡态理论:化学反应并不是通过简单的碰撞就能完成的,而是在反应物到生成物的过程中经过一个高能量的过渡态。如图是NO2和CO反应生成CO2和NO过程中的能量变化示意图,说明这个反应是(填“吸热”或“放热”)反应,NO2和CO的总能量(填“>”、“<”或“=”)CO2和NO的总能量。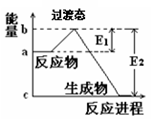
(2)在某体积为2L的密闭容器中充入0.5mol NO2和1mol CO,在一定条件下发生反应:
NO2+CO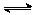 CO2+NO,2 min时,测得容器中NO的物质的量为0.2 mol ,则:
CO2+NO,2 min时,测得容器中NO的物质的量为0.2 mol ,则:
①该段时间内,用CO2表示的平均反应速为。
②假设此反应在5 min时达到平衡,则此时容器内气体的总物质的量为。
③下列事实能够说明上述反应在该条件下已经达到化学平衡状态的是
| A.容器内气体的质量保持变 | B.NO2的物质的量浓度不再改变 |
| C.容器内气体的平均相对分子质量不变 | D.NO2的消耗速率与CO2的消耗速率相等 |
E.容器内气体的物质的量保持不变
由A、B、C、D四种金属按下表中装置进行实验。
| 装置 |
(Ⅰ)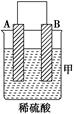 |
(Ⅱ)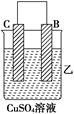 |
(Ⅲ)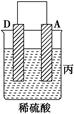 |
| 现象 |
二价金属A不断溶解 |
C的质量增加 |
A上有气体产生 |
根据实验现象回答下列问题:
(1)装置甲中负极的电极反应式是_______________________________________。
(2)装置乙中正极的电极反应式是_______________________________________。
(3)装置丙中溶液的pH________(填“变大”、“变小”或“不变”)。
(4)四种金属活泼性由强到弱的顺序是________。
某温度时,在2 L密闭容器中某一反应的A、B物质的量随时间变化的曲线如图所示,由图中数据分析求得:
(1)该反应的化学方程式为__________________________________。
(2)反应开始至4 min时,A的平均反应速率为________。
(3)4 min时,正、逆反应速率的大小关系为:v(正)________(填“>”、“<”或“=”,下同)v(逆),8 min时,v(正)________v(逆)。