2011年是国际化学年(IYC2011),其宗旨是"增进公众对化学重要性的认识,鼓励青年人热爱化学,学习和研究化学"。某校化学兴趣小组的同学,对课本中一氧化碳还原氧化铁实验作了绿色化改进后制取单质铁(
,
是活塞):

(1)关闭
、开启
,可以验证
还原
的产物。
①这是关于气体的实验,实验前必须对装置进行
②
还原
的化学方程式为
③在e处点燃气体的目的是
(2)关闭
,开启
,可以将
口出来的气体再从a通人装置而循环使用。
①
瓶中应装
②反应完后(假设b瓶中
全部转化为纯碱),要从
瓶中溶液得到纯碱固体,必要的实验操作为转移、
③该实验这样改进的主要优点是
万州中学初三一班的学生为了探究实验室中久置的氢氧化钠固体的成分,进行了有关实验,请你与他们一起完成以下探究活动。
【对固体猜想】Ⅰ:全部是NaOH;Ⅱ:全部是Na2CO3;Ⅲ:。
【查阅资料】经查阅资料可知,常见的盐溶液中,Na2CO3溶液显碱性,CaCl2溶液显中性
【实验和推断】
(1)向无色溶液中加入A溶液,现象a为有气泡产生,则A溶液是,说明氢氧化钠已经变质。
(2)由(1)可知氢氧化钠已经变质,重新取适量的无色溶液,加入足量的A(CaCl2溶液)除去Na2CO3,请写出这二者反应的化学方程式, 当实验现象(提示:现象a和b),则猜想Ⅲ成立。
实验小组帮助老师配置25℃(KNO3的溶解度为40g)时KNO3的饱和溶液,以备全班实验使用。老师提供的药品是含有少量NaCl的KNO3固体。(6分)
(1)查阅了两种物质的溶解度曲线,如图所示。40℃时溶解度大的是,将此温度下两物质的饱和溶液降温到10℃,此时溶质质量分数大的是。KNO3中混有少量NaCl的提纯方法是,用此法获得了足量的KNO3固体。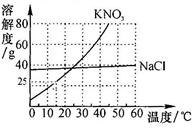
(2)配置100gKNO3饱和溶液的过程如下
①.计算。
②.称量:准确称量KNO3固体g(保留至0.1g); 称取过程中,发现指针已偏向右侧,接下来的操作是。
③.量取:用量筒量取蒸馏水。
④.溶解:将KNO3固体和水分别加入大烧杯中, 搅拌使固体完全溶解。
(3)若小组同学最后配得的KNO3溶液溶质的质量分数偏小,可能的原因是()
①.用量筒量取水时俯视读数②.配制溶液时烧杯用少量蒸馏水润洗③.在托盘天平的左盘放砝码,右盘放KNO3称量④.天平称量时,指针偏向左盘药品⑤.将固体倒入烧杯时有部分洒出
| A.①④ | B.②④⑤ | C.②③⑤ | D.②⑤ |
某校化学实验室废液桶中收集了溶解大量FeSO4、CuSO4的废水,若直接排放到下水道不仅造成重金属污染而且造成浪费。初三某班的同学,准备运用刚学到的“常见金属活动性顺序表”结合其他有关化学知识对废水进行处理。
(1)回忆常见金属活动顺序表,在下表空格中分别填入对应的元素符号。
(2)设计除去铜离子,回收硫酸亚铁晶体和铜的实验方案,讨论有关问题: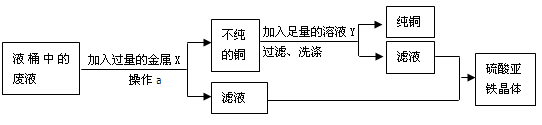
①操作a的名称是:,进行操作a使用玻璃棒的作用是。
②金属X是(填化学式,下同),有关反应的化学方程式为。
溶液Y是,利用其除去铜中杂质,有关反应的化学方程式为。
(6分)牙膏中的填充剂一般为碳酸钙、二氧气硅、氢氧化铝,其中“黑妹”牙膏用的填充剂是碳酸钙,请你设计实验验证其填充剂是碳酸钙,完成下列实验报告:
| 实验操作步骤 |
实验现象和结论 |
(5分)有一包粉末,可能由NaCl、MgCl2、FeCl3、Na2CO3、Na2SO4中的一种或几种组成。为了探究该粉末的组成,进行了如下实验:
(1)取样加水溶解,得到无色透明溶液。
(2)取(1)所得溶液少许,加入NaOH溶液,观察,没有明显现象。
(3)另取少量粉末,滴加稀盐酸,观察,也没有明显现象。
根据上述实验可得到的结论是:原粉末一定不含,可能含有的物质是。