向体积为2 L的密闭容器中充入2 mol SO2和1 mol O2,测得起始容器压强为p,一定条件下发生反应:2SO2(g)+O2(g) 2SO3(g) △H=-196 kJ·mol-1,维持容器温度不变,测得平衡时容器内压强为0.7p,若此时再向容器中充入2 mol SO3,则下列说法正确的是
2SO3(g) △H=-196 kJ·mol-1,维持容器温度不变,测得平衡时容器内压强为0.7p,若此时再向容器中充入2 mol SO3,则下列说法正确的是
| A.充入2 mol SO3后,SO2的物质的量增大 |
| B.第一次反应达到平衡时共放出热量176.4 kJ |
| C.充入2 mol SO3达到新平衡时,容器内的压强为1.4p |
| D.降低容器的温度可使新平衡时各物质的体积分数与第一次平衡时相同 |
下列反应一定有沉淀生成的是
| A.将SO2通入BaCl2溶液中 | B.将Cl2 通入AgNO3溶液中 |
| C.将CO2通入Ba(OH)2溶液中 | D.将NO2通入Ca(OH)2溶液中 |
用下图所示装置进行实验,下列对实验现象的解释不合理的是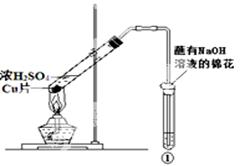
| ①中试剂 |
①中现象 |
解释 |
|
| A |
Ba(NO3)2溶液 |
生成白色沉淀 |
生成白色BaSO3沉淀 |
| B |
品红溶液 |
溶液褪色 |
SO2具有漂白性 |
| C |
紫色石蕊溶液 |
溶液变红 |
SO2与水反应生成酸 |
| D |
酸性KMnO4溶液 |
紫色褪去 |
SO2具有还原性 |
Cl2是纺织工业中常用的漂白剂,Na2S2O3可作为漂白布匹后的“脱氯剂”。S2O32-和Cl2反应的产物之一为SO42-。下列说法中,不正确的是
| A.该反应中氧化剂是Cl2 |
| B.根据该反应可判断还原性:S2O32->Cl- |
| C.上述反应中,每生成l mol SO42-,转移4 mol电子 |
| D.SO2与氯气的漂白原理相同,所以也可以用SO2做纺织工业的漂白剂 |
欲检验CO2气体中是否含有SO2、HC1,进行如下实验: ①将气体通入硝酸酸化的AgNO3溶液中,产生白色沉淀a;②滤去沉淀a,向滤液中加入Ba(NO3)2溶液,产生白色沉淀b。下列说法正确的是
| A.沉淀a为AgC1 | B.沉淀b为BaCO3 |
| C.气体中含有SO2 | D.气体中没有HC1 |
下列陈述Ⅰ、Ⅱ均正确且有因果关系的是
| 选项 |
陈述Ⅰ |
陈述Ⅱ |
| A |
SiO2有导电性 |
SiO2可用于制备光导纤维 |
| B |
Fe3+有氧化性 |
FeCl3溶液可溶解废旧电路板中的铜 |
| C |
NH3有还原性 |
NH3可用H2SO4吸收 |
| D |
浓HNO3有酸性 |
浓HNO3不可用铁制容器盛放 |