化学平衡原理在工农业生产中发挥着重要的指导作用。
(1)反应C(s)+CO2(g)  2CO(g)平衡常数K的表达式为;
2CO(g)平衡常数K的表达式为;
已知C(s) + H2O(g) CO(g)+H2(g)的平衡常数为K1;H2(g)+CO2(g)
CO(g)+H2(g)的平衡常数为K1;H2(g)+CO2(g)  CO(g)+H2O(g)的平衡常数为K2 ,则K与K1、K2二者的关系为。
CO(g)+H2O(g)的平衡常数为K2 ,则K与K1、K2二者的关系为。
(2)已知某温度下,反应2SO2+O2 2SO3,的平衡常数K=19
2SO3,的平衡常数K=19
在该温度下的体积固定的密闭容器中,c0(SO2)=1mol·L-1,c0(O2)="1" mol·L-1,当反应在该温度 下SO2转化率为80%时,该反应(填“是”或“否”)达到化学平衡状态,若未达到,向(填“正反应”或“逆反应”) 方向进行。
下SO2转化率为80%时,该反应(填“是”或“否”)达到化学平衡状态,若未达到,向(填“正反应”或“逆反应”) 方向进行。
(3)对于可逆反应:aA(g) +bB(g)  cC(g)+dD(g)△H = a kJ·mol-1;若a+b>c+d,增大压强平衡向_______(填“正反应”或“逆反应”)方向移动;若升高温度,平衡向逆反应方向移动,则a_______0(填“>”或“<”)
cC(g)+dD(g)△H = a kJ·mol-1;若a+b>c+d,增大压强平衡向_______(填“正反应”或“逆反应”)方向移动;若升高温度,平衡向逆反应方向移动,则a_______0(填“>”或“<”)
已知多元弱酸在水溶液中的电离是分步进行的,且第一步电 离程度远大于第二步电离程度,第二步电离程度远大于第三步电离程度……
离程度远大于第二步电离程度,第二步电离程度远大于第三步电离程度……
今有HA、H2B、H3C三种一元、二元、三元弱酸,
根据“较强酸 + 较弱酸盐 = 较强酸盐 + 较弱酸”的反应规律,它们之间能发生下列反应:
① HA + HC2-(少量)= A- + H2C-;
② H2B(少量)+2A- = B2- + 2HA;
③ H2B(少量)+ H2C- = HB- + H3C
回答下列问题:
(1)相同条件下,HA、H2B、H3C三种酸中酸性最强的是_________。
(2)A-、B2-、C3-、HB-、H2C-、HC2-六种离子中,最易结合质子(H+)的是_____,最难结合质子的是_____。
(3)完成下列反应的离子方程式
④ H3C + A-:_____________________;⑤ HB- + A-:______________________;
⑥ H3C + B2-:_____________________。
已知化学反应①:Fe(s)+CO2(g) FeO(s)+CO(g),其平衡常数为K1;化学反应②:Fe(s)+H2O(g)
FeO(s)+CO(g),其平衡常数为K1;化学反应②:Fe(s)+H2O(g)  FeO(s)+H2(g),其平衡常数为K2,在温度973 K和1 173 K情况下,K1、K2的值分别如下:
FeO(s)+H2(g),其平衡常数为K2,在温度973 K和1 173 K情况下,K1、K2的值分别如下:
| 温度 |
K1 |
K2 |
| 973 K |
1.47 |
2.38 |
| 1173 K |
2.15 |
1.67 |
(1)通过表格中的数值可以 推断:反应①是(填“吸热”或“放热”)反应。
推断:反应①是(填“吸热”或“放热”)反应。
(2)现有反应③:CO2(g)+H2(g)  CO(g)+H2O(g),请你写出该反应的平衡常数K3的数学表达式:K3=,根据反应①与②可推导出K1、K2与K3之间的关系式,据此关系式及上表数据,也能推断出反应③
CO(g)+H2O(g),请你写出该反应的平衡常数K3的数学表达式:K3=,根据反应①与②可推导出K1、K2与K3之间的关系式,据此关系式及上表数据,也能推断出反应③ 是(填“吸热”或“放热”)反应。
是(填“吸热”或“放热”)反应。
(3)要使反应③在一定条件下建立的平衡向正反应方向移动同时υ正增大可采取的措施
有(填写字母序号)。
A.缩小反应容器的容积 B.扩大反应容器的容积
C.升高温度 D.使用合适的催化剂 E.设法减小平衡体系中的CO的浓度
(4)图甲、乙分别表示反应③在t1时刻达到平衡,在t2时刻因改变某个条件而发生变化的情况:
①图甲中t2时刻发生改变的条件是。②图乙中t2时刻发生改变的条件是。
(5)在830℃温度下,反应③的K值为1,在2 L的密闭容器中,加入1 mol CO2和3 mol H2充分反应达平衡时,CO平衡浓度为mol/L。H2转化率。若向容器中再加入1 mol CO2和3 mol H2 达到平衡后CO平衡浓度mol/L ,CO2体积分数
(1)液化气中的主要成分之一是丁烷。在25℃、101 kPa时,10 kg丁烷完全燃烧生成CO2和H2O(l)放出热量5×105 kJ,丁烷燃烧的热化学方程式为____________________________丁烷的燃烧热为_________________。
(2)1 mol气态钠离子和1 mol气态氯离子结合生成1 mol氯化钠 晶体释放出的热能为氯化钠晶体的晶格能。
晶体释放出的热能为氯化钠晶体的晶格能。
①下列热化学方程式中,能直接表示出氯化钠晶体晶格能的是____________。
| A.Na+(g)+Cl-(g)―→NaCl(s);△Q | B.Na(s)+Cl2(g)―→NaCl(s);△Q1 |
| C.Na(s)―→Na(g);△Q2 | D.Na(g)-e-―→Na+(g);△Q3 |
E.Cl2(g)―→Cl(g);△Q4 F.Cl(g)+e-―→Cl-(g);△Q5
②写出△Q1与△Q、△Q2、△Q3、△Q4、△ Q5之间的关系式____
Q5之间的关系式____
(14分)
(1)25 ℃时,将pH=11的NaOH溶液与pH=4的硫酸溶液混合,若所得混合溶液pH=9,则NaOH溶液与硫酸溶液的体积比为
已知25 ℃时,0.1 L 0.1 mol·L-1的NaA溶液的pH=10,溶液中各离子的物质的量浓度由大到小的顺序为。
(2))若100 ℃时,KW=10-12,则100 ℃时pH=11的Ba(OH)2溶液与pH=2的硫酸按体积比1:9混合充分反应后pH=;若该温度下10体积的pH=a的某强酸溶液与1体积pH=b的某强碱溶液混合后溶液呈中性,则混合之前,a与b之间应满足的关系为 。
。
(3)某温度下的水溶液中,c(H+)=10x mol/L,c(OH-)=10y mol/L。x与y的关系如图所示。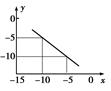
该温度下水的离子积为。该温度下氯化钠溶液的pH为
该温度下0.01 mol/L NaOH溶液的pH为。