X、Y、Z、W均为中学化学的常见物质,一定条件下它们之间有如图转化关系(其它产物已略去),下列说法不正确的是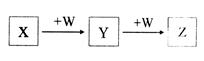
A.若 W是单质铁,则Z溶液可能是 W是单质铁,则Z溶液可能是 FeCl2溶液 FeCl2溶液 |
| B.若W是氢氧化钠,则X与Z可反应生成Y |
| C.若X是碳酸钠,则W可能是盐酸 |
| D.若W为氧气,则Z与水作用(或溶于水)一定生成一种强酸 |
下列所述变化规律正确的是
| A.Na、Mg、Al还原性依次增强 |
| B.HCl、PH3、H2S稳定性依次减弱 |
| C.NaOH、KOH、CsOH碱性依次增强 |
| D.S2-、Cl-、K+、Ca2+离子半径依次增大 |
如图所示,夹子开始处于关闭状态,将液体A滴入试管②与气体B充分反应,打开夹子,可发现试管①内的水立刻沸腾了。则液体A和气体B的组合不可能是下列的
| A.氢氧化钠溶液、二氧化碳 | B.盐酸、氨气 |
| C.氢氧化钠溶液、一氧化碳 | D.石灰水、二氧化硫 |
下列离子方程式中正确的是
| A.氨水与亚硫酸溶液混合:NH3·H2O+H+=NH4++H2O |
| B.SO2通入漂白粉溶液中:Ca(ClO)2+SO2+H2O=CaSO3↓+2HClO |
C.铜与浓硫酸共热:Cu+4H++SO42- Cu2++SO2↑+2H2O Cu2++SO2↑+2H2O |
| D.把H2S通入CuSO4溶液中:H2S+Cu2+=CuS↓+2H+ |
下列各组离子能大量共存的是
| A.Na+、Ba2+、S2-、SO32- | B.H+、K+、HSO3-、S2- |
| C.Fe2+、H+、Cl-、NO32- | D.K+、NH4+、SO42-、NO3- |
下列事实与浓硫酸具有强氧化性有关的是
①常温时用铁制容器运输浓硫酸
②硫酸工业生产中,用浓硫酸吸收SO3
③浓硫酸使蔗糖炭化变黑并有大量气体产生
④浓硫酸用于生产磷肥
⑤浓硫酸不能用来干燥HBr
| A.①③④ | B.①②③ | C.①③⑤ | D.②③④⑤ |