现有浓度均为0.1 mol/L的下列溶液:①硫酸、②醋酸、③氢氧化钠、④氯化铵、⑤醋酸铵、⑥硫酸铵、⑦硫酸氢铵、⑧氨水,请回答下列问题:
(1)①、②、③、④四种溶液中由水电离出的H+浓度由大到小的顺序是(填序号)_____.
(2)④、⑤、⑦、⑧四种溶液中NH浓度由大到小的顺序是(填序号)________.
(3)将①和⑧等体积混合后,混合液中各离子浓度关系正确的是________.
| A.c(H+)>c(SO)>c(NH)>c(OH-) |
| B.c(H+)=c(SO)=c(NH)>c(OH-) |
| C.c(NH)>c(H+)=c(SO)>c(OH-) |
| D.c(OH-)>c(H+)>c(NH)=c(SO) |
考生注意:23题为分叉题,分A、B两题,考生可任选一题。若两题均做,一律按A题计分。A题适合使用二期课改新教材的考生解答,B题适合使用一期课改教材的考生解答。
(A)现有部分短周期元素的性质或原子结构如下表:
| 元素编号 |
元素性质或原子结构 |
| T |
M层上有2对成对电子 |
| X |
最外层电子数是次外层电子数的2倍 |
| Y |
常温下单质为双原子分子,其氢化物水溶液呈碱性 |
| Z |
元素最高正价是+7价 |
(1)元素T的原子最外层共有 种不同运动状态的电子。元素X的一种同位素可测定文物年代,这种同位素的符号是
(2)元素Y与氢元素形成一种离子YH4+,写出该微粒的电子式 (用元素符号表示)
(3)元素Z与元素T相比,非金属性较强的是 (用元素符号表示),下列表述中能证明这一事实的是
a.常温下Z的单质和T的单质状态不同 b.Z的氢化物比T的氢化物稳定
c.一定条件下Z和T的单质都能与氢氧化钠溶液反应
(4)探寻物质的性质差异性是学习的重要方法之一。T、X、Y、Z四种元素的最高价氧化物的水化物中化学性质明显不同于其他三种酸的是 ,理由是
。
(B)现有部分短周期元素的性质或原子结构如下表:
| 元素编号 |
元素性质或原子结构 |
| T |
单质能与水剧烈反应,所得溶液呈弱酸性 |
| X |
L层p电子数比s电子数多2个 |
| Y |
第三周期元素的简单离子中半径最小 |
| Z |
L层有三个未成对电子 |
(1)写出元素X的离子结构示意图 。
写出元素Z的气态氢化物的电子式 (用元素符号表示)
(2)写出Y元素最高价氧化物水化物的电离方程式
(3)元素T与氯元素相比,非金属性较强的是 (用元素符号表示),下列表述中能证明这一事实的是
a.常温下氯气的颜色比T单质的颜色深
b.T的单质通入氯化钠水溶液不能置换出氯气
c.氯与T形成的化合物中氯元素呈正价态
(4)探寻物质的性质差异性是学习的重要方法之—。T、X、Y、Z四种元素的单质中化学性质明显不同于其他三种单质的是 ,理由 。
以石油裂解气为原料,通过一系列化学反应可得到重要的化工产品增塑剂
。
请完成下列各题:
(1)写出反应类型:反应①反应④
(2)写出反应条件:反应③反应⑥
(3)反应②③的目的是:。
(4)写出反应⑤的化学方程式:。
(5)
被氧化成
的过程中会有中间产物生成,该中间产物可能是(写出一种物质的结构简式),检验该物质存在的试剂是。
(6)写出
的结构简式。
一定条件下,在体积为3
的密闭容器中,一氧化碳与氢气反应生成甲醇(催化剂为
):
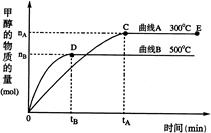
根据题意完成下列各题:
(1)反应达到平衡时,平衡常数表达式
=,升高温度,
值(填"增大"、"减小"或"不变")。
(2)在500℃,从反应开始到平衡,氢气的平均反应速率
=
(3)在其他条件不变的情况下,对处于E点的体系体积压缩到原来的1/2,下列有关该体系的说法正确的是
a.氢气的浓度减少 b.正反应速率加快,逆反应速率也加快
c.甲醇的物质的量增加 d.重新平衡时
增大
(4)据研究,反应过程中起催化作用的为
,反应体系中含少量
有利于维持催化剂
的量不变,原因是:(用化学方程式表示)。
乙基香草醛( )是食品添加剂的增香原料,其香味比香草醛更加浓郁。
)是食品添加剂的增香原料,其香味比香草醛更加浓郁。
(1)写出乙基香草醛分子中两种含氧官能团的名称。
(2)乙基香草醛的同分异构体A是一种有机酸,
可发生以下变化:
提示:①
②与苯环直接相连的碳原子上有氢时,此碳原子才可被酸性
溶液氧化为羧基
(a)由
的反应属于填反应类型)
(b)写出
的结构简式。
(3)乙基香草醛的另一种同分异构体
(
- -
)是一种医药中间体,请设计合理方案用茴香醛(
-
-
)是一种医药中间体,请设计合理方案用茴香醛(
- -
)合成
(其他原料自选,用反应流程图表示,并注明必要的反应条件)。例如:
-
)合成
(其他原料自选,用反应流程图表示,并注明必要的反应条件)。例如:



 -
-
工业上对海水资源综合开发利用的部分工艺流程如下图所示。
(1)电解饱和食盐水常用离子膜电解槽和隔膜电解槽,离子膜和隔膜均允许通过的分子或离子是。电解槽中的阳极材料为。
(2)本工艺流程中先后制得
、
和
,能否按
、
、
的顺序制备?原因是。
(3)膜在四氧化碳中的溶解度比在水中大得多,四氧化碳与水不互溶,故可用于萃取溴,但在上述工艺中却不用四氧化碳,原因是