下图中每一方框代表一种反应物或生成物: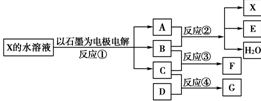
(1)若X由M、N两种短周期且同周期元素组成,M原子的最外层电子数比最内层电子数少1,N元素最高正价与它的最低负价代数和为6。反应④的数据如表格所示且D、G在常温下均为气体。
| |
C |
D |
G |
| 起始 |
3 mol |
1 mol |
0 |
| 3 min时 |
2.4 mol |
0.8 mol |
0.4 mol |
①写出反应②的离子方程式___________________________________________。
②物质G与F反应所形成盐的水溶液中离子浓度由大到小的顺序为______________。
(2)若X是一种含氧酸盐,B是金属单质,C、D是非金属单质,反应②需要B与A的浓溶液共热才能进行,且生成的E和G是同一种物质。写出反应①的化学方程式_________。
1 g固态D在C中完全反应放出9.3 kJ的热量,写出该反应的热化学方程式________。
甲乙两人分别用不同的方法配制100mL 0.92 mol/L的稀硫酸。
⑴甲:量取mL98﹪密度为1.84g/cm3的浓硫酸,小心地倒入成有少量水的烧杯中,搅拌均匀再转移到100mL容量瓶中,用少量的水将烧杯玻璃棒洗涤2-3次,将每次洗涤液也转移到容量瓶中,然后小心地向容量瓶中加水 定容,塞好瓶塞,反复上下摇匀。
定容,塞好瓶塞,反复上下摇匀。
①将溶液转移到容量瓶中的正确操作是
;
②定容的正确操作是。
⑵乙:用100mL量筒量取所需体积的浓硫酸,并向其中小心地加入少量的水,均匀搅拌待冷却至室温后,再加入水至100mL刻度线,再搅拌均匀。
你认为此法是否正确?若不正确,指出其中的错误之处
。
(12分)利用如下图的装置来做下面的实验: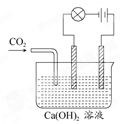
(1)先在玻璃容器里盛半杯Ca(OH)2溶液,然后由导管向容器溶液里通入CO2气体。随着CO2的通入,电灯就渐渐变暗,通入一定量时,电灯几乎完全熄灭,原因是 __________________________,如果继续通入CO2气体,电灯又会逐渐亮起来,原因是__________________________。在通入CO2的同时,能观察到溶液发生的现象是________________________,有关反应的离子方程式为_________________________。
(2)如果用氯化氢气体代替CO2气体,则观察到灯泡亮度变化是_________。有关离子反应方程式____________。
现有下列四种物质:Na2SO4、BaSO4、蔗糖(C12H22O11)、H2SO4,按照一定的依据,能找出一种物质与其它三种物质不同,从而分成两类。请你试试看,一共能找出多少种分法,把分类的依据和结果写在下面(至少填三种)
| 与其它三种不同的物质 |
分类依据 |
⑴通常状况下,甲同学取1 mol H2O加热到100℃时,液态水会汽化为水蒸气(如图所示),该过程属于变化。
在保持压强不变的情况下,水蒸气的体积22.4L 。(填“>”、“<”或“=”)
⑵乙同学做H2在O2中燃烧的实验,该实验过程属于变化,
在该变化过程中,一定保持相等的是(填序号)。
| A.反应物分子数目与生成物分子数目 |
| B.反应物原子总物质的量与生成物原子总物质的量 |
| C.反应物总质量与生成物总质量 |
| D.反应物体积与生成物体积 |
雄黄(As4S4)和雌黄(As2S3)是提取砷的主要矿物原料,二者在自然界中共生。根据题意完成下列填空:
(1) As2S3和SnCl2在盐酸中反应转化为As4S4和SnCl4并放出H2S气体。写出此反应的化学方程式。
(2)上述反应中的氧化剂是,氧化产物是 。
。
(3) As2S3和HNO3有如下反应:As2S3+ 10HNO3=2H3AsO4+ 3S+10NO2↑+ 2H2O
若生成1mol H3AsO4,则反应中转移电子的物质的量为。
(4)在3Cu + 8HNO3= 3Cu(NO3)2 + 2NO↑+4H2O的反应中,有6.4g铜被氧化,参加反应的HNO3的质量是____________g,被还原的HNO3的质量是__________g。
(5)在一定条件下,P bO2与Cr3+反应,产物是Cr2O72-和Pb2+,则生成1mol C
bO2与Cr3+反应,产物是Cr2O72-和Pb2+,则生成1mol C r2O72-
r2O72-
反应所需PbO2的物质的量为__________ ____。
____。