某化学小组围绕燃烧与灭火的主题开展了相关活动。请你参与完成:
【知识回忆】可燃物燃烧的必备条件是 ;
【交流讨论】(1)改进后的装置(如图二)与图一相比,其优点是 。欲使图二中的红磷着火,可将试管从水中取出并 后才能对试管加热;
(2)将装有某气体的大试管口朝下垂直插入水中,使试管罩住白磷(如图三所示),结果观察到了“水火相容”的奇观,则大试管所装气体可能是 ;
【综合应用】“水火不相容”是指水能灭火,其实水有时也可以“生火”,比如钾遇水会立刻着火,因为钾遇水生成H2和一种碱,该反应是 (填“吸热”或“放热”)反应,其反应化学方程式为 。
小徐和老师共同完成以下两个实验探究。
【探究一】酸和碱反应的探究
(1)请依据下图设计一个酸和碱反应的探究实验:
| 实验步骤 |
实验现象 |
结论 |
| ①向烧杯中加入10mL氢氧化钠溶液,并滴入几滴酚酞溶液; ②再用滴管慢慢滴入稀硫酸,并不断搅拌溶液。 |
①溶液颜色__________; ②不断搅拌溶液至溶液颜色恰好变成_____色为止。 |
酸和碱发生了中和反应,该反应属四种基本反应类型中的______反应。 |
(2)小徐选取BaCl2、酚酞、紫色石蕊溶液设计实验,分别探究上述酸、碱反应后烧杯中的硫酸是否过量,请你根据下表判断正确的实验方案及分析方案错误的原因:
| 实验方案 |
实验步骤 |
实验现象 |
实验结论 |
| 方案一 |
取样,滴入适量的氯化钡溶液 |
出现白色沉淀 |
硫酸过量 |
| 方案二 |
取样,滴入几滴无色酚酞溶液 |
酚酞溶液不变色 |
酸、碱恰好反应 |
| 方案三 |
取样,滴入几滴紫色石蕊溶液 |
溶液变红 |
硫酸过量 |
①设计的三个方案中,有一个正确的方案是:方案。
②请分析另外两个方案错误的原因:;。
【探究二】对实验室制取二氧化碳后的废液进行探究
(3)小徐取大理石和稀盐酸反应后的废液50g,逐滴加入碳酸钠溶液。根据实验测得的数据绘出右图,其中纵坐标m是实验得到的沉淀或气体的质量,横坐标表示加入的碳酸钠溶液的质量。请你参与回答下列问题:
①图中oa段表示生成的质量。
②通过计算求出图中b点溶液的溶质质量分数。(写出计算过程,最终结果保留至小数点后一位)
市售“管道通”能使堵塞的管道畅通。小华通过实验对“管道通”中的物质成分进行了探究。
【提出问题】“管道通”中含有什么物质?
【查阅资料】(1)下水管里的淤积物主要为油污、食物残渣、毛发等。
(2)氢氧化钠是强碱,能去除油污、腐蚀毛发等,可用于疏通管道。
(3)铝粉为银灰色固体,铝与酸、碱溶液都能反应放出氢气,并放出大量热。例如,铝与盐酸反应的化学方程式是, 铝与氢氧化钠溶液反应的化学方程式是2Al+2NaOH +2H2O====2NaAlO2 +3H2↑ 。
【猜想与验证】小华打开一盒“管道通”,内有一袋白色固体颗粒和一袋银灰色粉末。
| 实验操作 |
实验现象 |
| ① 将几粒白色固体颗粒放在表面皿上,放置一会儿 |
|
| ② 将几粒白色固体颗粒放入盛有少量水的试管中,并用手触摸试管外壁 |
|
| ③ 向操作②得到的溶液中放入一段羊毛线,加热一段时间 |
羊毛线逐渐消失 |
猜想Ⅰ:白色固体颗粒为氢氧化钠。
结论:白色固体颗粒为氢氧化钠。
猜想Ⅱ:银灰色粉末为铝粉。
| 实验操作 |
实验现象 |
①按照下图安装两套装置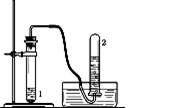 |
|
| ②向两套装置的试管1中分别依次加入银灰色粉末和稀盐酸、银灰色粉末和 |
都产生无色气体,试管1外壁温度明显升高 |
| ③待导管口有气泡均匀持续冒出时,收集一试管气体,验纯(两套装置操作相同) |
验纯时的操作和现象: |
| ④在导管口点燃气体(两套装置操作相同) |
都产生淡蓝色火焰 |
结论:银灰色粉末为铝粉。
【交流与反思】(1)老师告诉小华,氢氧化钾和氢氧化钠的性质非常相似。因此,要确认猜想Ⅰ是否正确,还需要学习如何检验钠元素的存在。
(2)使用管道通时,先将其中银灰色粉末添加于被堵塞的管道中,然后再加入白色固体颗粒,倒入一杯水后立即堵上管道口,管道内迅速发生反应。请写出一个使用“管道通”时的注意事项:
。
用加热氯酸钾和二氧化锰的方法来制取氧气,当收满一瓶气体后,停止加热。小军对试管中的剩余固体的成分做如下猜想①是氯酸钾②是氯化钾③是氯化钾和二氧化锰。三种猜想中一定不成立的是请你再做一个可能的猜想④是若 你的猜想正确请完成你的证明实验。
| 实验方案 |
实验现象 |
结论 |
| 猜想④正确 |
化学课外兴趣小组的同学利用图甲提供的四种试剂,探究图乙所示的相关实验(要求每种试剂只能使用一次)。
(1)若试管里是水,要证明CO2能与水发生化学反应,应加入下列药品中的,(填序号,下同)反应的化学方程式是。
(2)若试管里装入的是NaOH溶液,要证明CO2与NaOH溶液已经发生了反应,可向反应后的溶液中加入下列药品中的,发生反应的化学方程为。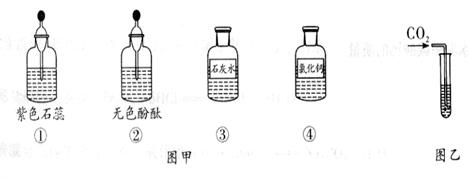
在煤矿的坑道里,若通风不好,遇有明火就会发生瓦斯爆炸事故,写出瓦斯气体(主要成分为甲烷)发生爆炸的化学方程式。
【提出问题】甲烷在空气中的含量占多少时,遇有明火一定会发生爆炸?
【查阅资料】甲烷在空气中的爆炸极限为含甲烷5%~15%.
【设计实验】取一个塑料瓶(容积575mL)、一支电子点火枪、胶塞,组装装置如图所示。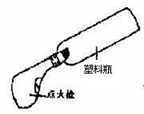
根据爆炸极限,取用30~70mL不同体积甲烷8份,每份都重复实验3次,实验结果如下:(注“√”表示发生爆鸣,“×”表示未发生爆鸣)
| 甲烷的体积(mL) |
30 |
40 |
45 |
50 |
55 |
60 |
65 |
70 |
|
| 占总体积的百分数(%) |
5.2 |
7.0 |
7.8 |
8.7 |
10.4 |
11.3 |
12.2 |
||
| 实验 次数 |
1 |
× |
√ |
× |
√ |
√ |
√ |
× |
× |
| 2 |
× |
× |
√ |
× |
√ |
√ |
× |
× |
|
| 3 |
× |
× |
× |
√ |
√ |
× |
√ |
× |
⑴每份都重复实验3次,目的是。
⑵分析上表,甲烷为mL,占总体积的百分数为%时,一定发生爆炸。
⑶甲烷占总体积的百分数在范围内可能会出现爆鸣现象。
⑷由实验分析可知当空气中含甲烷5%~15%,点燃时是否一定会发生爆炸?。(填“一定”或“不一定”)
⑸分析上述实验中未发生爆炸的原因(写出一条)。