(8分)某化学兴趣小组用一氧化碳与氧化铁的反应来探究炼铁的原理,装置如下图所示。请回答有关问题: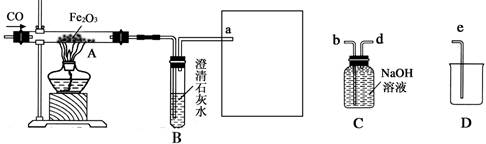
(1)为避免一氧化碳污染空气,并回收利用一氧化碳,方框中连接的是C和D,导管接口的连接顺序为a→( )→( )→( )。C装置中NaOH的作用是
(2)实验开始时,应 (填“先加热再通CO”或“先通CO再加热”),目的是 。
(3)实验进行一段时间后,玻璃管A中出现的现象为 ,反应方程式为 。
(4)除CO外,还有哪些物质可以还原Fe2O3 (请写一物质的化学式)。
化学课上老师向盛有NaOH溶液的试管中滴入2—3滴无色酚酞试液,振荡溶液呈红色。
提出问题:是什么微粒使无色酚酞变红?
查阅资料:NaOH溶液中主要存在H2O、OH-、Na+三种粒子。
猜想:①水分子使无色酚酞变红;
②Na+使无色酚酞变红;
③______使无色酚酞变红。
实验验证:
| 实验操作 |
现象 |
结论 |
| 实验一:分别向盛有NaOH溶液和蒸馏水的试管中滴入2—3滴无色酚酞试液 |
NaOH溶液中滴入酚酞后变红,蒸馏水中滴入酚酞后无现象。 |
猜想_______不成立。 |
| 实验二:_______________ |
________________________。 |
猜想②不成立。 |
| 实验三:分别向盛有NaOH溶液和石灰水的试管中滴入2—3滴无色酚酞试液 |
两支试管中滴入酚酞后均____。 |
猜想③成立。 |
在学习碱的化学性质时,某小组同学进行了如图所示的实验。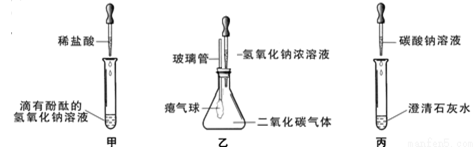
Ⅰ.探究碱的化学性质
①实验甲,随着稀盐酸的不断滴入,观察到溶液由红色变为无色;
②实验乙滴加氢氧化钠溶液后,观察到的气球变鼓;
③实验丙观察到试管内有白色沉淀产生,发生反应的化学方程式为(1)。
Ⅱ.探究废液成分
实验结束后,同学们将甲、乙、丙三个实验的废液倒入同一个干净的废液缸中,最终看到废液浑浊并呈红色,由此产生疑问。
【提出问题】废液中含有哪些物质?
【查阅资料】BaCl2溶液呈中性且Na2CO3 +BaCl2 ==BaCO3↓ +2NaCl
【讨论交流】
①废液中一定含有的物质:碳酸钙、指示剂、水和(2);
②还含有能使废液呈碱性的物质,同学们有如下猜想:
猜想1:碳酸钠;
猜想2:氢氧化钠;
猜想3:氢氧化钠和碳酸钠;
猜想4:氢氧化钠和氢氧化钙。
【查阅资料】BaCl2溶液呈中性,Na2CO3+BaCl2=BaCO3↓+2NaCl
【实验设计】
同学们认为需要先验证猜想4是否成立,所需要的试剂是(3)。
若猜想4不成立,则需要进行后续实验,请你完成表格。
实验操作预计现象预计结论
_______(4)__________ _________(5)__________猜想1正确
若没有白色沉淀,溶液呈红色猜想2正确
_________(6)____________猜想3正确
【进行实验】同学们进行实验,通过观察实验现象,得出了猜想2成立。
【反思拓展】分析化学反应后所得物质成分时,除考虑生成物外还需考虑反应物是否有剩余。
(5分)某兴趣小组发现一袋永川松花蛋的泥料,配料表上的成分是氧化钙、纯碱和食盐。他们要探究在腌制松花蛋过程中都有哪些物质对鸭蛋起作用。于是取少量泥料在水中溶解,充分搅拌后过滤,取滤液探究其成分。
【猜想与假设】他们都认为滤液中一定确NaCl和NaOH。对滤液中的其他成分他们分别做出了如下猜想:
甲同学:还可能有
乙同学:还可能有
 和
和
丙同学:还可能有
泥料在水中溶解,充分搅拌后生成氢氧化钠的化学方程式为。
【理论验证】大家讨论后认为同学的猜想是错误的。
【活动与探究】甲同学取一定量的滤液于试管中,向其中通入足量C02振荡,没有沉淀
产生,于是他得出结论:没有 。
。
丙同学取少量滤液于试管中,向其中滴加足量氯化钙溶液,振荡,产生现象,证明丙同学的猜想是正确的,发生反应的化学方程式为 。
日常生活中使用的塑料袋,有的是用聚乙烯制成的,有的是用聚氯乙烯制成的.小凤对包装食品的塑料袋进行探究,以验证其成分.
【作出猜想】①该塑料袋是用聚乙烯制成的;
②该塑料袋是用聚氯乙烯制成的;
【查阅资料】聚乙烯燃烧生成二氧化碳和水;聚氯乙烯燃烧生成二氧化碳、水和氯化氢;无水硫酸铜是白色粉末,遇水变为蓝色.
【实验探究】小凤将装置按A、B、C、D顺序连接好后,进行实验.在实验过程中,B、D产生明显现象,C无明显现象,说明塑料袋没有气体生成(填化学式).B装置的作用是;D瓶中发生反应的化学方程式是.
【实验结论】通过实验证明,猜想是正确的.
【交流反思】①从化学角度分析,大量使用塑料制品会导致.
②连接实验仪器时,将B、C位置能否进行交换,理由是。
某校兴趣小组同学准备进行常见酸、碱、盐的性质实验时,发现实验台上摆放的药品中(如下图),有一瓶溶液的试剂瓶未盖瓶盖且标签破损,于是决定对这瓶溶液进行实验探究:
【提出问题】这瓶溶液是什么溶液?
【获得信息】酸、碱、盐的性质实验中用到含有钠元素的物质是氯化钠、氢氧化钠、碳酸钠
【提出猜想】这瓶溶液是:猜想一:氯化钠溶液;猜想二:氢氧化钠溶液;猜想三:碳酸钠溶液。
【实验推断】(1)小丽取样滴加无酚酞试液,溶液呈红色,得出结论:该溶液不可能是溶液。
(2)小刚另取样滴加稀盐酸有产生,小刚得出结论:该溶液是碳酸钠溶液。
(3)小青认为小刚的结论不完全正确,理由。
小组同学讨论后一致认为还需要进行如下实验:
【继续探究】另取样加入过量的CaCl2溶液,观察到有产生,设计这一步骤的目的是;静置后,取上层清液,滴入酚酞试液,溶液呈红色。
【实验结论】这瓶溶液是。
【探究启示】实验取完药品后应。