在火箭推进器中装有强还原剂肼(N2H4)和强氧化剂(H2O2),当它们混合时,即产生大量的N2和水蒸气,并放出大量热。已知0.4mol液态肼和足量H2O2反应,生成氮气和水蒸气,放出256.65kJ的热量。
(1)写出该反应的热化学方程式__________________________________________。
(2)已知H2O(l)=H2O(g) △H=+44kJ·mol-1,则16 g液态肼和足量H2O2反应,生成氮气和液态水时,放出的热量是________kJ。
(3)上述反应应用于火箭推进剂,除释放大量的热和快速产生大量气体外,还有一个很突出的优点是________________________。
(4)已知N2(g)+2O2(g)="2" NO2(g) △H="+67.7" kJ·mol-1, N2H4(g)+O2(g)= N2(g)+2H2O (g) △H="-534" kJ·mol-1,根据盖斯定律写出肼与NO2完全反应生成氮气和气态水的热化学方程式______________________ ____。
一定温度下在10L容器中加入5molSO2和3molO2,当反应达到平衡时,有3molSO2发生了反应,则:
(1)生成了_________molSO3,SO2的转化率为_________(用百分数表示)。
(2)平衡时容器内气体的总物质的量为_________。
(3)平衡时SO2的浓度是_________ ,O2的浓度是_________,SO3的浓度是_________ 。
下列反应属于放热反应的是_______;属于吸热反应的是_______
| A.锌粒与稀H2SO4反应制取H2 | B.氢气在氧气中燃烧 |
| C.碳酸钙高温分解成氧化钙和二氧化碳 | D.氢氧化钾和硫酸中和 |
E.Ba(OH)2·8H2O与NH4Cl反应F. C与CO2高温生成CO
G.葡萄糖在人体内氧化分解 H.钢铁制品生锈的反应
A、B、C是短周期元素中的三种相邻元素,A、B为同周期元素,B、C为同主族元素,A、B、C的核外电子数之和为31。请回答下列问题:
(1)A、B、C的元素名称分别为:_________,_________,________;
(2)写出由A元素组成单质的电子式_________,画出C离子的结构示意图:_________;
(3)用电子式表示C的氢化物的形成过程。
在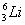 、
、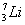 、
、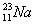 、
、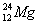 、
、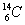 、
、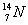 中:
中:
(1)和互为同位素;
(2)和的质量数相等,但不能互称同位素;
(3)和的中子数相等,但质子数不等,所以不是同一种元素
乙炔是有机合成工业的一种原料。工业上常用CaC2与水反应生成乙炔。
(1)CaC2中的C22-与O2 2+、N2互为等电子体,N2的结构式为O22+的电子式可表示为;1mol O22+中含有的π键数目为
2+、N2互为等电子体,N2的结构式为O22+的电子式可表示为;1mol O22+中含有的π键数目为
(2)将乙炔通入[Cu(NH3)2]Cl溶液生成Cu2C2红棕色沉淀。Cu+基态核外电子排布式为
(3)乙炔与氢氰酸反应可得丙烯腈(H2C=CH-C=N). 丙烯腈分子中所有碳原子轨道杂化类型为;分子中处于同一直线上的原子数目最多为。