为检验炭粉与浓硫酸反应的产物设计如下装置,回答相关问题: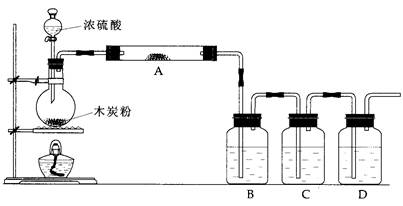
(1)上述装置中,在反应前用手掌紧贴烧瓶外壁检查装置的气密性,如观察不到明显的现象,还可以用什么简单的方法证明该装置不漏气
(2)写出浓硫酸和木炭粉在加热条件下发生反应的化学方程式:
(3)如果用图中的装置检验上述反应的全部产物,写出下面标号所表示的仪器中应加入的试剂的名称及其作用
A中加入的试剂和作用是______ _____
B中加入的试剂和作用是____ ____________
D中加入的试剂和作用是__ ___________
(4)实验时,C中应观察到的现象是______________________
实验室有一瓶Na2SO3固体,可能含有NaCl、Na2SO4、BaCl2、K2CO3、K2SO4中的一种或几种杂质,通过下列实验确定该样品的成分及Na2SO3的质量分数。请回答下列问题:
已知:
①取少量样品于试管中,加水振荡,未见沉淀生成:
②通过元素分析仪器的检测,得知该样品中不含K元素;
③用下图所示仪器进行合理组装,测定产生气体的体积(SO2在硫酸中的溶解忽略不计)
(1)按气流从左到右方向,正确的连接顺序为:A接____,接,接B。
(2)利用所组装置,由分液漏斗向烧瓶中滴加l0mL水,理论上将排入量筒中mL液体。
(3)液体X是,其作用是。
(4)Y的作用是防止产生的气体溶于水,下列历给试剂符合要求的是____(填序号)。
A.甲苯 B.四氯化碳 C.酒精 D.浓硫酸
若称取样品3.00g,加入10.0mol/L的硫酸至过量(共5mL),产生无色气体,排入量筒中液体的体积为229mL(已折算成标准下的状况)。根据此信息,回答以下问题:
(5)对实验获得准确的气体体积无益的操作有(填序号)
①检查装置的气密性:
②实验结束后,将连通ZJ、丁的导管中的水也引入量筒;
③读数时视线与量筒内凹液面最低相切点水平;
④恢复到室温后再上下调整量筒位置,使乙、丁两液面相平;
⑤在甲装置胶塞上再连接一个导管,通入N2将系统中SO2全部排出。
(6)向充分逸出气体后的溶液中加入过量BaCl2溶液,得到白色沉淀13.98g。根据实验所得现象及数据,可知:样品中Na2SO3的质量分数是,含有的杂质是。
为研究温度对Cl2与KOH反应的影响,设计实验如下:
在蒸馏烧瓶中装入足量MnO2,分液漏斗中装足量浓盐酸,大试管A中装4mol/LKOH溶液15mL,并置于75℃水浴中,大试管B中装02mol/LKOH溶液,并置于冰水中,C中装NaOH溶液。
试回答下列问题:
(1)水浴加热有什么优点?
(2)如何判断A中已经反应完全?
(3)分离A中生成的两种盐,检测发现其中KCl为005mol(不考虑HCl挥发),写出A中发生的化学方程式
(4)分离B中生成的两种盐, 其物质的量之比为1:1,写出离子方程式。
其物质的量之比为1:1,写出离子方程式。
(5)试管B要置于冰水中降温的主要原因是:
| A.从试管A中出来的气体温度较高,易使试管B中的溶液温度升高 | |
| B.防止生成的盐分解 | C.催化剂在冷水中活性最强 |
| D.该反应是放热反应,为防止温度过高,采用降温 |
(6)图一中,分液漏斗下端连接玻璃管并伸入液面下,其作用是什么? 可以用图二代替吗?。
可以用图二代替吗?。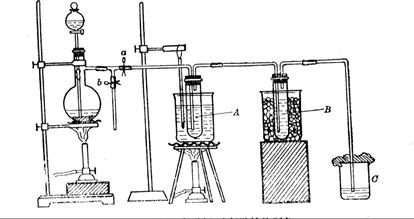
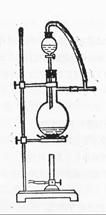
图一图二
Fe(OH)2由于在空气中易被氧化,制取时很难观察到白色沉淀现象,只能看到灰绿色,采用右图装置使用Fe,H2SO4(稀),NaOH溶液可在还原性气氛中制取Fe(OH)2白色沉淀,且较长时间内不变色,其中C为弹簧夹。(提示:还原性气氛如氢气环境)
(1)则锥形瓶A中应加入的药品为_________________.
(2)锥形瓶B中应加入的药品为__________________.
(3)容器A中的反应开始后,请简单写出完成制备Fe(OH)2的后续操作步骤。
①_____________________②_______________________________。
(4)若在反应开始之前先关闭弹簧夹C,则实验现象为:
;
请写出此时B瓶中发生的化学反应的离子方程式:
;
喷泉实验是一个有趣实验。现有250mL的烧瓶充满某种气体进行实验。设玻璃导管长35cm,胶 头滴管中可挤出0.50mL水。(不考虑溶质的损失)
头滴管中可挤出0.50mL水。(不考虑溶质的损失)
(1)0.5mL水中至少要溶解毫升该气体(标准状况),水才能从尖嘴管喷出(假设水面保持不变)?
(2)下列气体能做成喷泉实验的是____。(少选、错选不计分)
| 气体 |
A |
B |
C |
D |
E |
| 溶解度(标况) |
2.6 |
40 |
5.8 |
10.2 |
23.1 |
(3)假设NO2能进行喷泉实验,实验后该烧瓶中溶液的物质的量浓度为多少?(保留两位有效数字)
化学实验室制取氯化氢气体的方法之一是将浓硫酸滴入浓盐酸中。
(1)请从下图中挑选所需仪器,在方框内画出用该方法制备、收集干燥氯化氢气体、尾气处理的装置简图,并在图中标明所用试剂。(仪器可重复使用,固定装置不必画出)(Ⅱ见第五页)
试管圆底烧瓶集气瓶烧杯普通漏斗量筒分液漏斗长颈漏斗导管橡胶塞橡皮管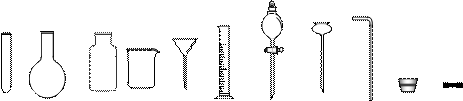

(2).(7分)实验室制备少量硫酸亚铁晶体的实验步骤如下:取过量洁净的铁屑,加入20%-30%的稀硫酸溶液,在50℃-80℃水浴中加热至不再产生气泡。将溶液趁热过滤,滤液移至试管中,用橡胶塞塞紧试管口,静置、冷却一段时间后收集产品。
①写出该实验制备硫酸亚铁的化学方程式:。
②采用水浴加热的原因是。
③硫酸溶液过稀会导致和。
④反应时铁屑过量的目的是(用离子方程式表示)。
⑤溶液趁热过滤的原因是。塞紧试管口的目的是。
⑥静置冷却一段时间后,在试管中观察到的现象是。