已知涤纶树脂的结构简式为: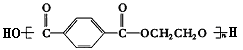 ,它是________和________(填单体的结构简式)通过____________反应而制的,反应的化学方程式为:______________________________________________。
,它是________和________(填单体的结构简式)通过____________反应而制的,反应的化学方程式为:______________________________________________。
(14分) 有A、B、C、D、E 五种元素的原子序数依次增大,B、C 的阳离子与A的阴离子和氖原子的电子层结构相同;A、B可形成离子化合物B2A;C的氧化物既能与强酸反应,又能与强碱反应;D的原子结构示意图为: ;E的最外层电子数是电子层数的2倍。试回答下列各问题:
;E的最外层电子数是电子层数的2倍。试回答下列各问题:
(1)B、D元素分别为、;
(2)D元素位于元素周期表中第周期、第族;
(3)化合物B2A的电子式____________________;
(4)E的最高价氧化物的水化物的分子式是________________________ 。
。
(5)D与NaOH溶液反应的化学方程式:_______________________________________。
(6)C的氧化物与E 的最高价氧化物的水化物溶液反应的离子方程式:
的最高价氧化物的水化物溶液反应的离子方程式:
_______________________________________________________________________。
(7分) 由Cl-、Br-、CO32-、SO32-、SO42-、Na+、Fe3+中若干种离子组成的化合物溶于水后得无色溶液,然后依次进行实验,观察到的现象记录如下:
①向溶液中加足量新制饱和的氯水,溶液变黄,无气体产生,再加入汽油振荡,静置,汽油层呈橙红色,用分液漏斗分离。
②向分液后所得的水溶液中加入BaCl2和盐酸的混合溶液,有白色沉淀产生,过滤。
③在滤液中加入AgNO3和HNO3的混合液,有白色沉淀产生。
请认真分析后回答下列问题:
(1)原溶液中是否含有Na+(填“是”“否”或“无法确定”,下同。),原溶液中是否含有Cl-。
(2)步骤①中溶液变黄的原因是(用离子方程式表示):
______________________________________________________________________。
(3)原溶液中是否含有SO32-、SO42-:(填“都有”、“都没有”、“仅有一种”或“至少有一种”)。理由是_____________________________________________________。
(10分) 用化学用语回答下列问题
(1)画出磷原子的原子结构示意图:。
(2)写出H2S分子的结构式:。
(3)用电子式表示MgCl2的形成过程:。
(4)用双氧水制取O2反应方程式。
(5)写出氢氧化铝与氢氧化钠溶液的离子反应方程式:
。
阿魏酸在医药、保健品、化妆品原料和食品添加剂等方面有着广泛的用途,其
结构简式为
⑴阿魏酸可以发生 (填选项字母)。"
a.酯化反应 b.消去反应 c.加成反应 d.氧化反应 e.银镜反应
⑵阿魏酸的一种同分异构体A 可用于制备有机玻璃(聚甲基丙烯酸甲酯),转化关系如下图所示:
己知A 和B都能与FeCl3溶液发生显色反应,B的一溴代物只有一种,A、C能发生银镜反应。
①B的结构简式为____________,C含有的官能团为____________。
②D→E的化学方程式为____________________________________。
③A的结构简式为__________________________________________。
(3)写出所有符合下列条件的阿魏酸的同分异构体的结构简式。
①苯环上有两个取代基,且苯环上的一漠代物只有2 种;
②能发生银镜反应;
③与碳酸氢钠溶液反应可放出使澄清石灰水变浑浊的气体;
④与FeCl3溶液发生显色反应__________________________________________。
在T1℃时,向容积为2 L 的密闭容器甲中加人1mol N1、3mol H2及少量固体催化剂,发生反应N2(g) + 3H2(g)  2NH3(g);△H<0,10min时各物质的浓度不再变化,测得NH3 的体积分数为25% 。
2NH3(g);△H<0,10min时各物质的浓度不再变化,测得NH3 的体积分数为25% 。
(1) 该反应在0 ~l0min 时间内H2的平均反应速率为______,N2的转化率为______。 (2)在T1℃时,若起始时在容器甲中加入0.5mol N2、1.5mol H2、0.5mol NH3 ,则达到平衡时NH3的体积分数______ (填选项字母) 。
(2)在T1℃时,若起始时在容器甲中加入0.5mol N2、1.5mol H2、0.5mol NH3 ,则达到平衡时NH3的体积分数______ (填选项字母) 。
a.大于25% b.等于25% c.小于25%
(3)右图是在T1℃时密闭容器甲中H2的体积分数随时间t的变化曲线,请在该图中补画出该反应在T2℃(T1>T2)时H2的体积分数随时间t的变化曲线。
(4)若保持T1℃,在体积也为2 L 的密闭容器乙中通入一定量的N2、H2、NH3,欲使平衡时容器乙中各物质的物质的量与容器甲中完全相同,且起始时反应向正反应方向进行,则通入H2的物质的量x的取值范围是____________。