已知:下列各种物质都由1~18号元素组成,它们之间的关系如下图所示。

常温下,A、F为金属单质,J是液体,F既能与L溶液反应,又能与N溶液反应。
C、H、M为气体单质,其中H呈黄绿色,A、B、I、K、L、R的焰色反应均呈黄色。
R的水溶液中滴加盐酸时,刚开始有白色沉淀,后来沉淀又逐渐溶解。
已知G是H2O2,H2O2在碱性条件下分解速率会加快。请回答:
(1)B为淡黄色固体,请写出B与J反应的离子方程式
(2)P不稳定易分解成N和C,该反应的化学方程式为
(3)请写出上述电解反应的化学方程式
(4)R与足量盐酸反应的离子方程式为
(5)F是常用于野外焊接无缝铁轨的原料,请写出焊接铁轨所发生的化学反应方程式:
(4分)同温同压下,等质量的钠分别与过量的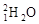 和过量的
和过量的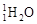 完全反应,所生成的氢气的体积比为,质量比为。
完全反应,所生成的氢气的体积比为,质量比为。
(8分)从短周期元素中找出满足下列条件的单质或化合物:
⑴跟水反应最剧烈的金属元素的单质是;跟水反应最剧烈的非金属元素的单质是;常温下有颜色的气体单质是。
⑵含氢质量分数最大的气态氢化物是;水溶液对玻璃有强烈腐蚀性的气态氢化物是;四核10电子粒子有。
(5分)1999年1月,俄美科学家联合小组宣布合成出114号元素(Uuq)的一种同位素,该原子的质量数是289,试回答下列问题:
⑴该元素在周期表中位于第周期族,属于金属元素还是非金属元素?。
⑵该原子核内中子数为。
⑶写出该元素最高价氧化物对应水化物的化学式。
(14)下表为元素周期表的一部分,列出了10种元素在元素周期表中的位置。试回答下列问题:
| ① |
|||||||||||||||||
| ⑥ |
⑦ |
||||||||||||||||
| ② |
④ |
⑤ |
⑧ |
||||||||||||||
| ③ |
⑩ |
||||||||||||||||
| ⑨ |
⑴②、③、④三种元素最高价氧化物的水化物的碱性由强到弱的顺序是(填化学式)。
⑵10种元素中,原子半径最小的是(填序号)。
⑶元素⑦的氢化物分别与②和⑧的单质反应的离子方程式为,
。
⑷元素②和⑤的最高价氧化物的水化物相互反应的化学方程式为。
⑸元素⑩的原子序数为,该元素在地壳中的含量居第四位,是目前应用最广泛的一种金属,其单质与⑧的氢化物的水溶液反应的离子方程式为。
⑹⑥与⑧形成化合物的化学式为;单质⑨溶于该化合物所得溶液呈色。
(6分)元素周期表中共有个横行,即个周期,其中长周期和短周期各个。除第1周期和第7周期外,每一周期的元素都是从元素开始,以元素结束。同一周期的主族元素,从左到右,原子半径逐渐,失电子能力逐渐,得电子能力逐渐;金属性逐渐,非金属性逐渐;最高价氧化物的水化物碱性逐渐,酸性逐渐。