短周期六元素A、B、C、D、E、F,原子序数依次增大;A、B的阴离子与C、D的阳离子的电子排布式均为ls22s22p6,A原子核外有2个未成对电子,C单质可与热水反应但不能与冷水反应;E、F原子在基态时填充电子的轨道有9个,且E原子核外有3个未成对电子,F能与A形成相同价态的阴离子,且A离子半径小于F离子。回答:
(1)写出各元素的符号:A B C D E F
(2)写出B与C形成的化合物的电子式
(3)请写出元素F的价电子排布式
(4)上述六种元素按电负性从小到大的排列是 (写元素符号)。
(5)C、D、E、F元素第一电离能最大的是 (写元素符号);
(6)C、D、E、F四种元素中,形成的最高价氧化物对应水化物中(写化学式):
酸性最强的是 碱性最强的是 呈两性的是
有下列物质:①CO2②N2③H2O2④NH3⑤Ca(OH)2⑥Na2O2⑦NH4Cl,试用以上物质的序号填空:
(1)既有极性键,又有非极性键的是______________;
(2)既有离子键,又有非极性键的是______________;
(3)属于共价化合物的是______________。
某兴趣小组的同学用如图所示装置研究有关电化学的问题(甲、乙、丙三池中溶质足量),当闭合该装置的电键K时,观察到电流计的指针发生了偏转。当乙池中C极质量减轻10.8 g时,回答下列问题。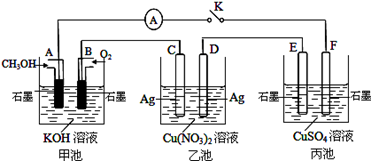
(1)写出A极的电极方程式:。
(2)甲池中B电极理论上消耗O2的体积(标准状况下)为多少毫升?
(3)若丙池中溶液的体积为1000 mL,此时丙池中溶液的pH为多少?
根据下列有机物转化流程回答: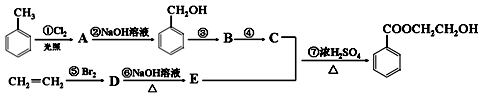
(1)写出A的结构简式: 。
(2)属于取代反应的有(填序号):。属于加成反应的有(填序号):。
(3)写出第①步反应的化学方程式:
____________________________________________________________________________
写出物质B与新制Cu(OH)2溶液反应的化学方程式:
___________________________________________________________________________
写出第⑥步反应的化学方程式:
___________________________________________________________________________
请根据所学化学知识回答下列问题:
(1)在浓度均为0.1 mol/L ①CH3COONH4、②NH4HSO4、③NH3·H2O、④(NH4)2SO4溶液中,NH4+浓度由大到小的顺序为(填序号)。
(2)氯化铝溶液蒸干,灼烧得到的固体物质是_________,用化学方程式说明其原因:
(3)某温度时蒸馏水的pH=6。将2.3 g金属钠放入该蒸馏水中,充分反应后再加该蒸馏水稀释到1 L,恢复到原温度时所得溶液的pH=。
已知某有机物的结构简式为: 。
。
(1)该有机物中所含官能团的名称是。
(2)该有机物发生加成聚合反应后,所得产物的结构简式为;
(3)写出该有机物发生消去反应的化学方程式(注明反应条件):
___________________________________________________________________________