工业上电解饱和食盐能制取多种化工原料,其中部分原料可用于制备多晶硅。
(1)下图是离子交换膜法电解饱和食盐水示意图,电解槽阳极产生的气体是 ;NaOH溶液的出口为 (填字母);精制饱和食盐水的进口为 (填字母);干燥塔中应使用的液体是 。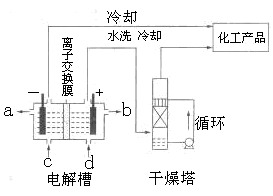
(2)多晶硅主要采用SiHCl3还原工艺生产,其副产物SiCl4的综合利用受到广泛关注。
① SiCl4可制气相白炭黑(与光导纤维主要原料相同),方法为高温下SiCl4与H2和O2反应,产物有两种,化学方程式为 。
② SiCl4可转化为SiHCl3而循环使用。一定条件下,在20L恒容密闭容器中的反应:
3 SiCl4(g)+2H2(g)+Si(s) 4SiHCl3(g)
4SiHCl3(g)
达平衡后,H2与SiHCl3物质的量浓度分别为0.140mol/L和0.020mol/L,若H2全部来源于离子交换膜法的电解产物,理论上需消耗纯NaCl的质量为 ______kg。
(3)采用无膜电解槽电解饱和食盐水,可制取氯酸钠,同时生成氢气,现制得氯酸钠213.0kg,则生成氢气 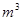 (标准状况)。
(标准状况)。
.已知锌与稀硫酸反应为放热反应,某学生为了探究其反应过程中的速率变化,用排水集气法收集反应放出的氢气,实验记录如下:
| 经过时间(min) |
1 |
2 |
3 |
4 |
5 |
| 氢气体积(mL) |
30 |
120 |
280 |
350 |
370 |
(1)①反应速率最大的(即0~1 min、1~2 min、2~3 min、3~4 min、4~5 min)时间段为 ,原因是 。
②反应速率最小的时间段为 ,原因是。
以甲醇、空气和氢氧化钾溶液为原料,金属铂为电极可构成普通的燃料电池。该电池的负极上的电极反应式为____________
在2L容器中3种物质间进行反应,X、Y、Z的物质的量随时间的变化曲线如图。反应在t时到达平衡,依图所示:
①该反应的化学方程式是 。
②反应起始至t,Y的平均反应速率是。
现有8种元素的性质、数据如下表所列,它们属于第二或第三周期。
回答下列问题:
(1)①在元素周期表中的位置是(周期、族);
(2)比较④和⑦的氢化物的稳定性(用化学式表示) ______。
(11分,每空1分)下表是元素周期表的一部分。根据表中的10种元素,用元素符号或化学式填空:
| 族 期 |
ⅠA |
ⅡA |
ⅢA |
ⅣA |
ⅤA |
ⅥA |
ⅦA |
0 |
| 1 |
① |
|||||||
| 2 |
② |
③ |
||||||
| 3 |
④ |
⑤ |
⑥ |
⑦ |
⑧ |
|||
| 4 |
⑨ |
⑩ |
(1)在①~⑩元素中,金属性最强的金属元素是________。
(2) 在①~⑩元素中,________(填化学式)的单质既可以和盐酸又可以和氢氧化钠溶液反应,其单质与氢氧化钠溶液反应的化学方程式是_______________________。
(3)在①~⑩元素中,形成的最高价氧化物的水化物的酸性最强的酸的分子式是________。
(4)④、⑥、⑦、⑨所形成的单核离子中,半径最大的离子是________。
(5)由表中两种元素的原子按1∶1组成的常见液态化合物的稀溶液易被催化分解,可使用的催化剂为(填序号)________。A.MnO2 B.FeCl3C.Na2SO3 D.KMnO4
(6)用电子式表示元素⑦与元素⑨形成的化合物的形成过程:。
用电子式表示元素⑥与元素①形成的化合物的形成过程:。
(7)①与③和①与⑥均能形成18个电子的化合物,此两种化合物发生反应的化学方程式为。
(8)比较⑩与⑦单质氧化性的强弱的反应的化学方程式是
比较②与⑥单质的非金属性的强弱的反应的化学方程式是