(8分)在实验室里,某同学取一小块金属钠做与水反应的实验。试完成下列问题:
(1) 切开的金属钠暴 露在空气中,最先观察到的现象是
露在空气中,最先观察到的现象是
,所发生反应的化学方程式是  。
。
(2) 将钠投入水中后,钠融化成一个小球,根据这一现象你能得出的结论是:
① ,② 。 将一小块钠投入盛有饱和石灰水的烧杯中,不可能观察到的现象是 (填编号)。
| A.有气体生成 |
| B.钠融化成小球并在液面上游动 |
| C.溶液底部有银白色的金属钙生成 |
| D.溶液变浑浊 |
(3) 在钠与水反应过程中,若生成标准状况下224mL的H2,则转移的电子的物质的量为 。
(4) 根据上述实验过程中钠所发生的有关变化,试说明将金属钠保存在煤油中的目的是 。
【化学——选修2:化学与技术】
电镀厂镀铜废水中含有CN-和Cr2O72-离子,需要处理达标后才能排放。该厂拟定下列流程进行废水处理,回答下列问题: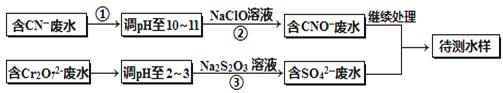
(1)上述处理废水流程中主要使用的方法是_________________;
(2)②中反应后无气体放出,该反应的离子方程式为______________;
(3)步骤③中,每处理0.4mol Cr2O72-时转移电子2.4mol,该反应的离子方程式为;
(4)取少量待测水样于试管中,加入NaOH溶液,观察到有蓝色沉淀生成,再加Na2S溶液,蓝色沉淀转化成黑色沉淀,请使用化学用语和文字解释产生该现象的原因;
(5)目前处理酸性Cr2O72-废水多采用铁氧磁体法。该法是向废水中加入FeSO4 ·7H2O将Cr2O72-还原成Cr3+,调节pH,Fe、Cr转化成相当于: (铁氧磁体,罗马数字表示元素价态)的沉淀。
(铁氧磁体,罗马数字表示元素价态)的沉淀。
处理1mol Cr2O72-,需加入a mol FeSO4 • 7H2O,下列结论正确的是_______。
| A.x ="0.5" ,a ="8" | B.x ="0.5" ,a =" 10" | C.x =" 1.5" ,a =8 | D.x =" 1.5" ,a = 10 |
(Ⅰ)甲醇是一种新型的汽车动力燃料,工业上可通过CO和H2化合来制备甲醇。
已知某些化学键的键能数据如下表:
| 化学键 |
C—C |
C—H |
H—H |
C—O |
C≡O |
H—O |
| 键能/kJ·mol-1 |
348 |
413 |
436 |
358 |
1072 |
463 |
请回答下列问题:
(1)已知CO中的C与O之间为叁键连接,则工业制备甲醇的热化学方程式为
;
(2)某化学研究性学习小组模拟工业合成甲醇的反应,在容积固定为2L的密闭容器内充入1 molCO和 2 molH2,加入合适催化剂(体积可以忽略不计)后在250°C开始反应,并用压力计监测容器内压强的变化如下:
| 反应时间/min |
0 |
5 |
10 |
15 |
20 |
25 |
| 压强/MPa |
12.6 |
10.8 |
9.5 |
8.7 |
8.4 |
8.4 |
则从反应开始到20min时,以CO表示的平均反应速率=,该温度下平衡常数K=,若升高温度则K值(填“增大”、“减小”或“不变”);
(3)下列描述中能说明上述反应已达平衡的是;
A.2 v (H2)正=" v" (CH3OH)逆
B.容器内气体的平均摩尔质量保持不变
C.容器中气体的压强保持不变
D.单位时间内生成 n molCO 的同时生成 2n molH2
(Ⅱ)回答下列问题:
(1)体积均为100mL pH=2的CH3COOH与一元酸HX,加水稀释过程中pH与溶液体积的关系如图所示,
则Ka(HX) ______ Ka(CH3COOH)(填>、<或=)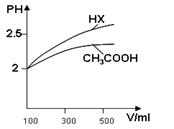
(2)25℃时,CH3COOH与CH3COONa的混合溶液,若测得pH=6,则溶液中C(CH3COO−)-c(Na+)=_________mol·L-1(填精确值)。
工业上为了测定辉铜矿(主要成分是Cu2S)中Cu2S的质量分数,设计了如图装置。实验时按如下步骤操作:
| A.连接好仪器,使其成为如图装置,并检查装置的气密性。 |
| B.称取研细的辉铜矿样品1.000g。 |
| C.将称量好的样品小心地放入硬质玻璃管中。 |
| D.以每分钟1L的速率鼓入空气。 |
E.将硬质玻璃管中的辉铜矿样品加热到一定温度,发生反应为:Cu2S+O2 SO2 +2Cu。
SO2 +2Cu。
F.移取25.00mL含SO2的水溶液于250mL锥形瓶中,用0.0100mol/L KMnO4标准溶液滴定至终点。按上述操作方法重复滴定2—3次。
试回答下列问题:
(1)装置①的作用是_________________;装置②的作用是____________________。
(2)假定辉铜矿中的硫全部转化为SO2,并且全部被水吸收,则操作F中所发生反应的化学方程式为,当产生_______________________________的现象时可判断滴定已经达到终点。
(3)若操作F的滴定结果如下表所示,则辉铜矿样品中Cu2S的质量分数是________。
| 滴定 次数 |
待测溶液的 体积/mL |
标准溶液的体积 |
|
| 滴定前刻度/mL |
滴定后刻度/mL |
||
| 1 |
25.00 |
1.04 |
21.03 |
| 2 |
25.00 |
1.98 |
21.99 |
| 3 |
25.00 |
3.20 |
21.24 |
(4)本方案设计中由一个明显的缺陷影响了测定结果(不属于操作失误),你认为是(写一种即可)。
(5)已知在常温下FeS 的 Ksp= 6 . 25 × 10 -18, H2S 饱和溶液中 c (H+)与 c (S2-)之间存在如下关系:c2 (H+)·(S2-) =" 1" . 0×10-22。在该温度下,将适量 FeS 投入硫化氢饱和溶液中,欲使溶液中(Fe2+)为1 mol/L,应调节溶液的c(H十)为__________________。
尿素[
]是首个由无机物人工合成的有机物.
(1)工业上尿素由
和
在一定条件下合成,其反应方程式为.
(2)当氨碳比
=4时,
的转化率随时间的变化关系如图1所示.
①A点的逆反应速率v逆(
)B点的正反应速率v正(
)(填"大于""小于"或"等于").
②NH3的平衡转化率为.
(3)人工肾脏可采用间接电化学方法除去代谢产物中的尿素,原理如图2所示.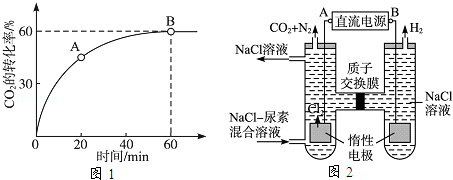
①电源的负极为(填"
"或"
").
②阳极室中发生的反应依次为、.
③电解结束后,阴极室溶液的pH与电解前相比将;若两极共收集到气体13.44
(标准状况),则除去的尿素为
(忽略气体的溶解).
衣康酸
是制备高效除臭剂、粘合剂等多种精细化学品的重要原料,可经下列反应路线得到(部分反应条件略).
(1)
发生加聚反应的官能团名称是,所得聚合物分子的结构型式是(填"线型"或"体型").
(2)
→
的化学方程式为.
(3)
的同分异构体
是饱和二元羧酸,则
的结构简式为(只写一种).
(4)已知:
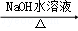 +
,
经五步转变成M的合成反应流程(如图1):
+
,
经五步转变成M的合成反应流程(如图1):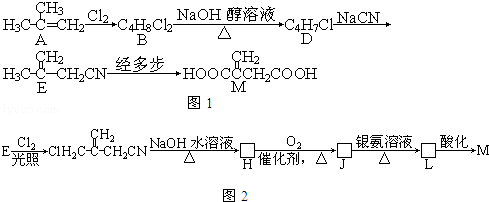
①
→
的化学反应类型为,
→
的化学方程式为.
②
→
的离子方程式为.
③已知:
 +
,
经三步转变成M的合成反应流程为(示例如图2;第二步反应试剂及条件限用
水溶液、加热).
+
,
经三步转变成M的合成反应流程为(示例如图2;第二步反应试剂及条件限用
水溶液、加热).