“低碳循环”引起各国的高度重视,而如何降低大气中CO2的含量及有效地开发利用CO2,引起了全世界的普遍重视。所以“低碳经济”正成为科学家研究的主要课题
(1)用电弧法合成的储氢纳米碳管常伴有大量的碳纳米颗粒(杂质),这种颗粒可用如下氧化法提纯,请完成该反应的化学方程式:
___ C+ ___ KMnO4+6 H2SO4 = ____CO2↑+ ____MnSO4 + ____K2SO4+ 6H2O
(2)将不同量的CO(g)和H2O(g)分别通入到体积为2L的恒容密闭容器中,进行反应
CO(g)+H2O(g) CO2(g)+H2(g),得到如下二组数据:
CO2(g)+H2(g),得到如下二组数据:
| 实验组 |
温度℃ |
起始量/mol |
平衡量/mol |
达到平衡所需时间/min |
||
| CO |
H2O |
H2 |
CO |
|||
| 1 |
650 |
4 |
2 |
1.6 |
2.4 |
6 |
| 2 |
900 |
2 |
1 |
0.4 |
1.6 |
3 |
①实验1中以v (CO2) 表示的反应速率为 (保留小数点后二位数,下同)。
②实验2条件下平衡常数K=_________,该反应为 (填“吸”或“放”)热反应。
(3)已知在常温常压下:
① 2CH3OH(l) + 3O2(g) = 2CO2(g) + 4H2O(g) ΔH = -1275.6 kJ/mol
② 2CO (g)+ O2(g) = 2CO2(g) ΔH = -566.0 kJ/mol
③ H2O(g) = H2O(l) ΔH = -44.0 kJ/mol
写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式:
⑷某实验小组依据甲醇燃烧的反应原理,设计如右图所示的电池装置。 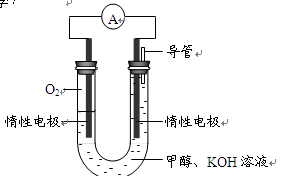
① 该电池正极的电极反应为
。
②该电池工作时,溶液中的OH-向______极移动。
(3分)在含有Al3+、Ba2+、Fe3+三种离子的混合溶液中只加一种试剂达到下列目的。所给的备选试剂有:氨水、NaOH溶液、H2SO4溶液、AgNO3溶液、Na2CO3溶液
(1)只让Ba2+离子沉淀完全,应加入________________;
(2)要让Al3+、Fe3+两种离子沉淀完全,应加入_________________;
(3)使三种离子全部转化为沉淀,应加入__________________________。
(3分)冶炼金属常用以下几种方法:① 以C或CO、H2作还原剂还原;② 电解法;③ 热分解法,现冶炼下列金属Al、Fe、Hg,试标明适宜的冶炼方法(填序号):
AlFeHg。
(1)在25°C时,纯水中C(H+)·C(OH-)=_________________;
(2)在NH4Cl溶液中C(H+)______10-7mol/L(大于、小于或等于),pH______7(大于、小于或等于);
(3)在Na2CO3溶液中C(H+)______10-7mol/L (大于、小于或等于),pH______7(大于、小于或等于)
(4)在NaCl溶液中C(H+)______10-7mol/L (大于、小于或等于),pH______7(大于、小于或等于).
铜是一种有色金属与人类关系非常密切。铜及其化合物在生产、生活中有广泛的应用。某同学对Cu的常见化合物的性质进行实验探究,研究的问题和过程如下:
(1)为探究不同价态铜的稳定性,进行如下实验:
向Cu2O中加适量稀硫酸,得到蓝色溶液和一种红色固体,该反应的离子化学方程式为_________;由此可知,在酸性溶液中,+2价Cu比+1价Cu更(填“稳定”或“不稳定”)。
(2)硫酸铜是一种应用广泛的化工原料,实验室中可通过不同途径制取硫酸铜溶液和胆矾(CuSO4·5H2O),其中一种流程如图:
①杂铜(含少量有机物)灼烧后的产物除氧化铜还含少量铜,原因可能是________(填字母代号)。
a.该条件下铜无法被氧气氧化 b.灼烧不充分.铜未被完全氧化
c.氧化铜在加热过程中分解生成铜 d.灼烧过程中部分氧化铜被还原
②若将杂铜换为纯净的铜粉,可直接向其中加入稀硫酸和Fe2(SO4)3溶液,不断通入氧气。反应完全后向其中加入过量________(填化学式,下同),调节pH至,生成沉淀,过滤得硫酸铜溶液。已知:
| 氢氧化物开始沉淀时的pH |
氢氧化物沉淀完全时的pH |
|
| Fe3+ |
2.7 |
3.7 |
| Fe2+ |
7.6 |
9.6 |
| Cu2+ |
4.7 |
6.7 |
(3)通过下述图1装置也可制取硫酸铜溶液(已知:2NaOH+2NO2=NaNO3+NaNO2+H2O)。
烧瓶内发生反应的化学方程式为__________________;
图2是图1的改进装置,
其优点有①____________________,②_________________ 。
(4)为测定CuSO4·5H2O晶体的纯度,进行下列实验:取a g试样配成l00 mL溶液,每次取20.00mL,消除干扰离子后,用b mol·L-1EDTA(Na2H2Y)标准溶液滴定其中的Cu2+(离子方程式为Cu2++H2Y2-=CuY2-+2H+),滴定至终点,平均消耗EDTA溶液l2.00 mL。(常温时,5%的Na2H2Y水溶液,其pH为4—6。)
①CuSO4·5H2O晶体的纯度是 。
②下列滴定方式中,最合理的是(夹持部分略去) (填序号)。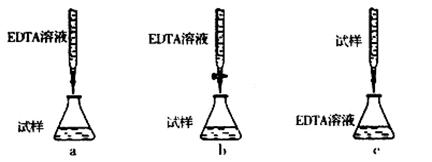
(10分)氨的合成是最重要的化工生产之一。
I.工业上合成氨用的H2有多种制取的方法:
① 用焦炭跟水反应:C(s)+ H2O(g)  CO(g)+ H2(g);
CO(g)+ H2(g);
② 用天然气跟水蒸气反应:CH4(g)+ H2O(g) CO (g)+ 3H2(g)
CO (g)+ 3H2(g)
已知有关反应的能量变化如下图,则方法②中反应的ΔH=_____________。
Ⅱ.在同温度下、使用相同催化剂分别进行反应:
3H2(g)+ N2(g) 2NH3(g),按不同方式在2L容器中投入反应物,保持恒温、恒容,反应达到平衡时有关数据为:
2NH3(g),按不同方式在2L容器中投入反应物,保持恒温、恒容,反应达到平衡时有关数据为:
| 容 器 |
甲 |
乙 |
丙 |
| 反应物投入量 |
3 mol H2、2 mol N2 |
6 mol H2、4mol N2 |
2 mol NH3 |
| 达到平衡的时间(min) |
t |
5 |
8 |
| 平衡时N2的浓度(mol·L-1) |
c1 |
1.5 |
|
| N2的体积分数 |
ω1 |
ω2 |
ω3 |
| 混合气体密度(g·L-1) |
ρ1 |
ρ2 |
(1)下列能说明该反应已达到平衡状态的是
a.容器内N2、H2、NH3的浓度之比为1︰3︰2b.v(N2)正=3v(H2)逆c.容器内压强保持不变d.混合气体的密度保持不变
(2)甲容器中达到平衡所需要的时间t 5min (填>、<或=)
(3)乙中从反应开始到平衡时N2的平均反应速率(注明单位)。
(4)分析上表数据,下列关系正确的是________。
a.2c1=1.5mol/Lb.ω1=ω2 c.2ρ1=ρ2
(5)该温度下,容器乙中,该反应的平衡常数K=______(用分数表示)。