下列物质中:⑴Na ⑵ Br2 ⑶NaCl溶液 ⑷CO2 ⑸蔗糖 ⑹NH3 ⑺Na2O
⑻H2S气体 ⑼BaSO4 ⑽NaCl固体 ⑾Ba(OH)2 。
属于电解质的是 , 属于非电解质的是 ,能导电的是 。(用序号填写)
某有机物A的结构简式如图:(1)某同学对其可能具有的化学性质进行了如下预测,其中错误 的是 。
的是 。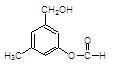
①可以使酸性高锰酸钾溶液褪色②可以和NaOH溶液反应
③在一定条件下可以和乙酸发生反应④在一定条件下可以发生消去反应
⑤在一定条件下可以和新制Cu(OH)2反应⑥遇FeCl3溶液可以发生显色反应
(2)该有机物的同分异构体甚多,其中有一类可以用 通式表示(其中X、Y均不为氢),试写出其中
通式表示(其中X、Y均不为氢),试写出其中 符合上述通式且能发生银镜反应的四种物质的结构简式:
符合上述通式且能发生银镜反应的四种物质的结构简式:
, , , ;
中性物质 A可发生下列变化,且B、D、E均可发生银镜反应,G的核磁共振氢谱中只有一个吸收峰。
A可发生下列变化,且B、D、E均可发生银镜反应,G的核磁共振氢谱中只有一个吸收峰。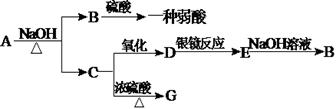
(1)  推断下述物质的结构简式:
推断下述物质的结构简式:
A:________________ D: ________________
(2)写出下列变化的化学方程式:
A+NaOH→B+C:_____________________________________________
C→G:________________________________________________
已知A、B、C、D、E是短周期中的五种非金属元素,它们的原子序数依次增大。五种元素中A元素原子半径最小;B原子的最外层电子数是内层电子数的2倍;E元素与D元素同主族;E的单质为黄色固体,自然界中游离态的E常出现在火山口附近。
(1)请写出元素符号:B;D。
(2)画出E的阴离子结构示意图。
(3)B、C两种元素对应的最高价含氧酸的酸性较强的是(填化学式)。
(4)A元素的单质和C元素的单质在一定条件下反应,生成化合物X。 X 的电子式为,向X的水溶液中滴入石蕊试液,会观察到的现象是。
(5)用电子式表示化合物BD2的形成过程。
(6)向苛性钠溶液中通入过量的A2E气体时,所发生反应的离子方程式为。
(7)化合物ED2与氯 气的水溶液充分反应可生成两种强酸,该反应的化学方程式
气的水溶液充分反应可生成两种强酸,该反应的化学方程式
为。
已知溴单质的氧化性介于氯和碘之间,利用这一性质解决下面问题。
(1)下列物质或微粒中,在酸性条件下可能氧化Br-的是(填序号)。
A.I2 B. MnO4- C.MnO2 D.Cl-
(2)把滤纸用淀粉和碘化钾的混合溶液浸泡、晾干后可获得实验常用的淀粉碘化钾试纸。这种试纸润湿后,遇少量氯气可观察到试纸变蓝,用化学方程式解释该现象: 。
(3)下列试剂不能把NaCl和KI两种无色溶液区别开的是(填序号)。
A.氯水B.溴水C.淀粉溶液 D.稀硝酸
(4)100mL溴化 亚铁溶液中通入3.36L氯气(标况),充分反应后测得溶液中氯离子与溴离子的物质的量浓度相等,则原溴化亚铁溶液的物质的量浓度为。
亚铁溶液中通入3.36L氯气(标况),充分反应后测得溶液中氯离子与溴离子的物质的量浓度相等,则原溴化亚铁溶液的物质的量浓度为。
将4 mol SO2和2 mol O2在2 L的密闭容器中混合,在一定 条件下发生如下反应:2SO2(g)+O2(g)
条件下发生如下反应:2SO2(g)+O2(g) 2SO3(g)。若经过2s后测得SO3的浓度为0.6 mol/ L,用氧气表示该反应2s内的平均速率V(O2)=;2s末O2浓度为;2s末SO2的转化率为。
2SO3(g)。若经过2s后测得SO3的浓度为0.6 mol/ L,用氧气表示该反应2s内的平均速率V(O2)=;2s末O2浓度为;2s末SO2的转化率为。