某重要的香料F其合成路线有多条,其中一条合成路线如下: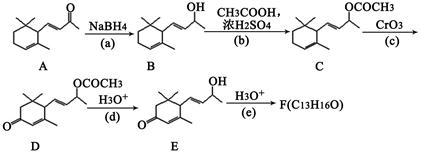
(1)在(a)~(e)的反应中,属于取代反应的是 。(填编号)
(2)化合物F的结构简式是 。
(3)在上述转化过程中,步骤(b)的目的是 。
(4)写出同时满足下列四个条件的D的两种同分异构体的结构简式 。
| A.该物质属于芳香族化合物 | B.该分子中有4种不同类型的氢原子 |
| C.1mol该物质最多可消耗2molNaOH | D.该物质能发生银镜反应 |
有一包白色固体,可能含有CaCO3、Na2SO4、KNO3、CuSO4、BaCl2五种物质中的一种或几种。现进行以下实验:
①取少量白色固体加到足量的水中,得到白色沉淀,上层清液为无色。
②向上述悬浊液中加入足量的稀硝酸,白色沉淀消失,并有气泡产生。
③取少量②的溶液滴入硝酸钡溶液,有白色沉淀生成,再加入稀硝酸,白色沉淀不消失。
根据上述实验现象判断:白色固体中一定含有,
一定不含有, 可能会有;
上述实验中有关反应的离子方程式。
下列各组中都有一种物质与其他物质在分类上不同,试分析每组物质的特点,将这种不同于其他物质的物质找出来。
(1)NaCl、KCl、NaClO、BaCl2:____
(2)HClO3、KClO3、Cl2、NaClO3:________
(3)H3PO4、H2SiO3、HCl、H2SO4:______
(4)空气、N2、HCl气体、CuSO4·5H2O:_______
下列物质属于电解质的是;能导电的物质是。
①氨水②蔗糖③烧碱④NH3·H2O⑤CO2⑥铜
(1)鉴别Fe(OH)3胶体和FeCl3溶液的方法是
(2)除去KNO3溶液中的I2杂质,主要操作步骤是:加CCl4后,振荡,静置,。水溶液最终从分液漏斗的分离出来
(3)黑火药是中国的“四大发明”之一。黑火药在发生爆炸时,发生如下的反应:
2KNO3+C+S=K2S+2NO2↑+CO2↑。其中被氧化的元素是,氧化剂是,生成1molCO2时转移的电子数目为(NA表示阿伏伽德罗常数的值)
硫酸是用途广泛的化工原料,可作脱水剂、吸水剂、氧化荆和催化剂等。
工业制硫酸铜的方法很多。
(1)方法一、用浓硫酸和铜制取硫酸铜。该反应的化学方程式是_____________________,此法的最大缺点是____________________________。
(2)方法二、用稀硫酸、铜和氧化铁制取硫酸铜,生产的主要过程如下图所示:
①稀硫酸、铜和氧化铁反应的离子方程式是__________________、________________;
向混合溶液中通入热空气的反应的离子方程式是_______________________________。
②请说出调整PH为4的目的是_______________________;由滤液得到无水硫酸铜的实验操作是______________________________。