A、B、C、D是中学化学的常见物质,其中A、B、C均含有同一种元素。在一定条件下相互转化的关系如下图所示(部分反应中的H2O已略去)。请填空: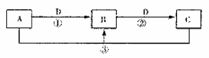
(1)若A可用于自来水消毒,D是生产、生活中用量最大、用途最广的金属单质,加热蒸干B的溶液不能得到B,则B的化学式可能是 ;工业上制取A的离子方程式为 。
(2)若A是一种碱性气体,常用作制冷剂,B是汽车尾气之一,遇空气会变色,则反应①的化学方程式为 。
(3)若D是氯碱工业的主要产品,B有两性,则反应②的离子方程式是 。
(4)若A、C、D都是常见气体,C是形成酸雨的主要气体,则反应③的化学方程式 。
(5)氯碱工业是高耗能产业,一种将电解池与燃料电池相组合的新工艺可以节(电)能30%以上。在这种工艺设计中,相关物料的传输与转化关系如下图所示,其中的电极未标出,所用的离子膜都只允许阳离子通过。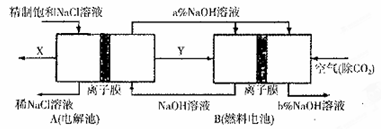
①图中X、Y分别是 、 (填化学式),分析比较图示中氢氧化钠质量分数a% b%(填“>”、“=”或“<”)
②写出燃料电池B中负极上发生的电极反应 。
(12分)
二甲醚是一种重要的清洁燃料,可替代氟利昂作制冷剂,对臭氧层无破坏作用。工业上可利用煤的气化产物(水煤气)合成二甲醚。请回答下列问题:
(1)利用水煤气合成二甲醚的总反应为: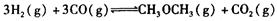
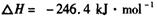
它可以分为两步,反应分别如下: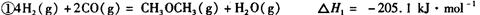
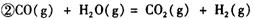
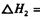 :__________________ ______________
:__________________ ______________
(2)在一定条件下的密闭容器中,该总反应达到平衡,只改变一个条件能同时提高反应速和CO的转化率的是_______(填字母代号)。
a.降低温度b.加人催化剂c.缩小容器体积
d.增加H2的浓度e.增加CO的浓度
(3)在一体积可变的密闭容器中充入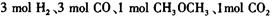 ,在一定温度和压强下发生反应:
,在一定温度和压强下发生反应: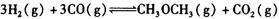 ,经一定时间达到平衡,并测得平衡时混合气体密度是同温同压下起始时的1.6倍。问:①反应开始时正、逆反应速率
,经一定时间达到平衡,并测得平衡时混合气体密度是同温同压下起始时的1.6倍。问:①反应开始时正、逆反应速率 的大小:V(正)____V(逆)(填“ >”、“ < ”或"="),理由是:________________________________
的大小:V(正)____V(逆)(填“ >”、“ < ”或"="),理由是:________________________________
②平衡时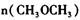 =_________________,平衡时CO的转化率= _________________。
=_________________,平衡时CO的转化率= _________________。
有关元素X、Y、Z、W的信息如下:
请回答下列问题:
(1) Y的单质在空气 中充分燃烧所得氧化物的电子式________________
中充分燃烧所得氧化物的电子式________________
(2) X、Y、W的简单离子的半径由大到小的是_______________ (写离子符号)
(3) 向淀粉碘化钾溶液中滴加几滴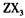 的浓溶液,现象为______________ ,
的浓溶液,现象为______________ ,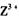 基态离子的电子排布式为
基态离子的电子排布式为
(4) 以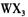 溶液为原料制取无水
溶液为原料制取无水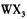 ,主要操作包括加热浓缩、冷却结晶、过滤,先制得
,主要操作包括加热浓缩、冷却结晶、过滤,先制得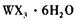 晶体,然后在条件下加热
晶体,然后在条件下加热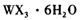 晶体,能进一步制取无水
晶体,能进一步制取无水 .其原因是(结合离子方程式简要说明) _____________________________________________
.其原因是(结合离子方程式简要说明) _____________________________________________
为了防治环境污染并对尾气进行综合利用,某硫酸厂用氨水吸收尾气中的SO2,再向吸收液中加入浓硫酸,以制取高浓度的SO2及(NH4)2SO4和NH4HSO4固体。
为了测定上述(NH4)2 SO4和NH4HSO4固体混合物的组成,现称取该样品四份,分别加入相同浓度的NaOH溶液各40.00mL,加热至120℃左右,使氨气全部逸出[(NH4)2SO4和NH4HSO4的分解温度均高于200℃],测得有关实验数据如下(标准状况):
SO4和NH4HSO4固体混合物的组成,现称取该样品四份,分别加入相同浓度的NaOH溶液各40.00mL,加热至120℃左右,使氨气全部逸出[(NH4)2SO4和NH4HSO4的分解温度均高于200℃],测得有关实验数据如下(标准状况):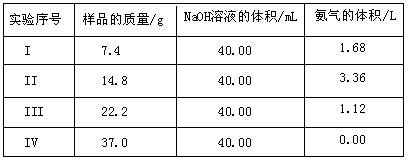
(1)实验过程中有关反应的离子方程式为
;
(2)由I组数据直接推测:标准状况下3.7g样品进行同样实验时,生成氨气的体积为
L;
(3)试计算该混合物中(NH4)2SO4和NH4HSO4的物质的量之比;
(4)欲计算该NaOH溶液的物质的量浓度应选择第组数据,由此求得NaOH溶液的物质的量浓度为。
已知A、B、C、D、E、F六种有机物存在如下转化关系, E在核磁共振氢谱中出现三组峰,其峰面积之比为6:1:1,F能使Br2的CCl4溶液褪色。回答下列问题: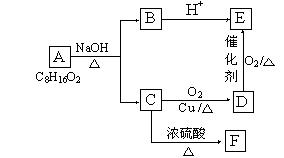
(1)C和E的官能团名称:C,E;
(2)由F生成高聚物的化学方程式
(3)六种有机物中能跟Na反应的是(填字母)
(4)由A生成B和C的化学反应方程式为
(5)D在一定条件下生成C的化学反应方程式为
根据下图所示的关系填空,已知A为FeS2固体,C的焰色反应火焰呈 黄色,其中①、③是硫酸工业生产中的重要反应,D、E常温下为气体,X常温下为无色液体,F是红棕色固体。
黄色,其中①、③是硫酸工业生产中的重要反应,D、E常温下为气体,X常温下为无色液体,F是红棕色固体。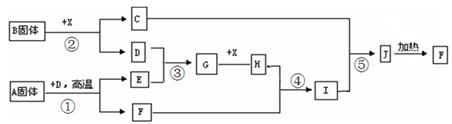
(1)物质X的化学式是 ____。
(2)化合物B中所包含的化学键有和 __。
(3)反应④的离子方程式为。
反应②的化学方程式为___ ___,其中还原剂是。
(4)已知每生成16克E,放出106.5KJ的热量,则反应①的热化学反应方程式为 ___。