下列微粒中,未成对电子数最多的是
| A.O:1s22s22p4 | B.P:1s22s22p63s23p3 |
| C.Cr:1s22s22p63s23p63d54s1 | D.Mn:1s22s22p63s23p63d54s2 |
下列反应中生成物总能量高于反应物总能量的是
| A.碳酸钙受热分解 | B.乙醇燃烧 |
| C.铝粉与氧化铁粉末反应 | D.氧化钙溶于水 |
下列说法不正确的是
| A.氢能、核能都是无污染的高效能源 |
| B.把煤转化为液态燃料可提高煤的燃烧效率 |
| C.推广使用太阳能、风能、海洋能,有利于缓解温室效应 |
| D.使用催化剂,能增大活化分子百分数,所以反应速率增大 |
已知Q与R的摩尔质量之比为9∶22,在反应X+2Y=2Q+R中,当1.6g X与Y完全反应后,生成4.4g R,则参与反应的Y和生成物Q的质量之比为( )
| A.46∶9 | B.32∶9 | C.23∶9 | D.16∶9 |
下列根据实验现象所得出的结论中,正确的是( )
| A.某物质焰色反应呈黄色,结论:该物质一定是钠盐 |
| B.无色试液加入NaOH溶液,加热产生的气体使湿润的红色石蕊试纸变蓝,结论:试液中一定含有NH4+ |
| C.无色溶液中加入BaCl2溶液有白色沉淀产生,再加盐酸,沉淀不消失,结论:原溶液一定含有SO42- |
| D.无色溶液中加入稀盐酸产生无色无味气体,该气体能使澄清石灰水变浑浊,结论:原溶液一定含有CO32- |
向盛有氯气的集气瓶中,注入约五分之一的下列液体并轻轻振荡,观察到的现象记录如图所示,判断瓶中注入的液体是()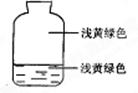
| A.AgNO3溶液 | B.NaOH溶液 |
| C.水 | D.石蕊溶液 |