已知A、B、C、D、E、F是含有同一种元素的化合物,其中F能使红色湿润石蕊试纸变蓝色,它们之间能发生如下反应:
① A+H2O → B+C ② C+F → D ③ D+NaOH → F+E+H2O
(1)写出它们的化学式:D ,F 。
(2)写出①反应的化学方程式: ,
此反应中氧化剂是 ,还原剂是 。
(3)写出反应③的离子方程式: 。
(4)工业生产C的过程中有如下一步反应:即F经催化氧化生成B和H2O,写出该步反应的化学方程式: 。
某汽车安全气囊的产气药剂主要含有
、
、
、
等物质。当汽车发生碰撞时,产气药剂产生大量气体使气囊迅速膨胀,从而起到保护作用。
(1)
是气体发生剂,受热分解产生
和
,
的电子式为。
(2)
是主氧化剂,与
反应生成的还原产物为(已知该反应为置换反应).
(3)
是助氧化剂,反应过程中与
作用生成
和
。
含有化学键的类型为,
的原子结构示意图为。
(4)
是冷却剂,吸收产气过程中释放的热量而发生分解,其化学方程式为。
(5)100
上述产气药剂产生的气体通过碱石灰后得到
33.6
(标准状况)。
①用碱石灰除去的物质为;
②该产气药剂中
的质量分数为。
物质结构与性质]碳及其化合物广泛存在于自然界中,回答下列问题:
(1)处于一定空间运动状态的电子在原子核外出现的概率密度分布可用形象化描述。在基态原子中,核外存在对自旋相反的电子。
(2)碳在形成化合物时,其键型以共价键为主,原因是。
(3)
分子中,共价键的类型有,
原子的杂化轨道类型是,写出两个与
具有相同空间构型和键合形式的分子或离子。
(4)
能与金属
形成
,该化合物的熔点为253
,沸点为376
,其固体属于晶体。
碳有多种同素异形体,其中石墨烯与金刚石的晶体结构如图所示:
①在石墨烯晶体中,每个
原子连接个六元环,每个六元环占有个C原子。
②在金刚石晶体中,
原子所连接的最小环也为六元环,每个
原子连接个六元环,六元环中最多有个
原子在同一平面。
、
、
、
为原子序数依次增大的四种元索,
和
具有相同的电子构型;
、
为同周期元索,
核外电子总数是最外层电子数的3倍;
元素最外层有一个未成对电子。回答下列问题:
(1)四种元素中电负性最大的是(填元素符号),其中
原子的核外电子排布式为。
(2)单质
有两种同素异形体,其中沸点高的是(填分子式),原因是;
和
的氢化物所属的晶体类型分别为和。
(3)
和
反应可生成组成比为1:3的化合物
,
的立体构型为,中心原子的杂化轨道类型为。
(4)化合物
的立体构型为,中心原子的价层电子对数为,单质D与湿润的
反应可制备
,其化学方程式为。
(5)
和
能够形成化合物
,其晶胞结构如图所示,晶胞参数,
=0.566
,
的化学式为:晶胞中
原子的配位数为;列式计算晶体F的密度(
)。
甲醇是重要的化工原料,又可称为燃料。利用合成气(主要成分为
、
和
)在催化剂的作用下合成甲醇,发生的主反应如下:
①

②

③

回答下列问题:
(1)已知反应①中的相关的化学键键能数据如下:
由此计算
=
,已知
=-58
,则
=
。
(2)反应①的化学平衡常数
的表达式为;图1中能正确反映平衡常数
随温度变化关系的曲线为(填曲线标记字母),其判断理由是。
(3)合成气的组成
=2.60时,体系中的
平衡转化率(
)与温度和压强的关系如图2所示。
值随温度升高而(填"增大"或"减小"),其原因是。图2中的压强由大到小为,其判断理由是。
随原子序数的递增,八种短周期元素(用字母
表示)原子半径的相对大小、最高正价或最低负价的变化如下图所示。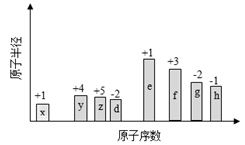
根据判断出的元素回答问题:
(1)
在元素周期表的位置是。
(2)比较
、
常见离子的半径的小(用化学式表示,下同)>;比较
、
的最高价氧化物对应的水化物的酸性强弱是:>。
(3)任选上述元素组成一种四原子共价化合物,写出其电子式。
(4)已知1
e的单质在足量
中燃烧,恢复至室温,放出255.5
热量,写出该反应的热化学方程式:。
(5)上述元素可组成盐
:
,向盛有10
1
溶液的烧杯中滴加1
溶液,沉淀物质的量随
溶液体积变化示意图如下: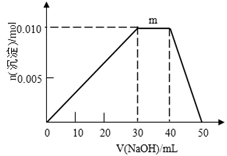
①
离子浓度由大到小的顺序是:。
②写出m点反应的离子方程式。
③若
溶液改加20
1.2
溶液,充分反应后,溶液中产生沉淀的物质的量为
。