制取氨气并完成喷泉实验(图中夹持装置均已略去)。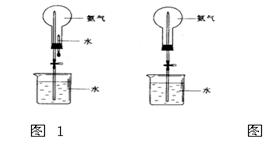
(1)写出实验室制取氨气的化学方程式: 。
(2)收集氨气应使用 法,要得到干燥的氨气可选用 做干燥剂。
(3)用图1装置进行喷泉实验,上部烧瓶已装满干燥氨气,引发水上喷的操作是 。该实验利用了氨气
的 性质。
(4)如果只提供如图2的装置,请说明引发喷泉的方法 。
下表为元素周期表的一部分,a、b、c…为部分元素。回答下列问题:
| a |
|||||||||||||||||
| b |
c |
d |
e |
||||||||||||||
| f |
g |
||||||||||||||||
| d |
h |
[ |
|||||||||||||||
(1)请写出上述元素h的基态原子核外电子排布式;
(2)比较e、g两种元素的气态氢化物的稳定性(写化学式);
(3)b2a4分子的结构式是,该分子中存在的σ键与π键的个数比为;
(4)c、d两种元素中第一电离能较大的是(写元素符号),其原因是;
(5)已知f的氢氧化物与水电离出的OH—可形成配位键,则生成的含有配位键的离子的结构简式为(标出配位键)。
(1)按要求填空:电负性最大的元素符号 ______;第一电离能最大的元素基态原子核外电子排布式_________;第三周期原子半径最小的元素的价电子排布式______。
(2)在下列物质中:①N2、②H2O、③NaOH、④MgCl2、⑤C2H4、⑥Na2O2(用序号填空)
其中只含有非极性键的是;只含有极性键的是;只含有离子键的是;既含有非极性键又含有极性键的是;含有非极性键的离子化合物是。
(3)N≡N的键能为942kJ·mol-1,N—N单键的键能为247kJ·mol-1,通过计算说明N2中的键更稳定(填“σ”或“π”)。
下表是某地市场上销售的一种“加碘盐”包装袋上的部分文字说明。请根据此表,结合初中学过的化学知识,回答下列问题:
| 配料表 |
精制海盐、碘酸钾(KIO3) |
| 含碘盐 |
20~40mg/kg |
| 储藏方法 |
密封避光、防潮 |
| 使用方法 |
烹调时待食品熟后加入碘盐 |
(1)碘酸钾属于哪类物质?(填:“纯净物”、“混合物”、“单质”、“氧化物”)
(2)根据含碘盐的食用方法,可推测碘酸钾的化学性质:碘酸钾在受热时
(3)我国规定,食盐含碘量为每千克食盐含碘0.035g,相当于每千克食盐含碘酸钾g。(列式表示,不必计算出最后的数值)
已知碳有两种常见的同位素126C、136C;氧有三种常见的同位素168O、178O、188O。
(1)由这五种微粒构成的CO的分子有种。
(2)本题中涉及种核素,种元素。
(3)一个相对分子质量最大的二氧化碳分子中有个电子,个中子;0.5 mol这种二氧化碳的质量是g。
单晶硅是制作电子集成电路的基础材料。科学家预计,到2011年一个电脑芯片上将会集成10亿个晶体管,其功能远比我们想象的要大的多,这对硅的纯度要求很高。用化学方法可制得高纯度硅,其化学方程式为:
① SiO2 + 2C Si + 2CO ② Si + 2Cl2
Si + 2CO ② Si + 2Cl2 SiCl4③ SiCl4 + 2H2
SiCl4③ SiCl4 + 2H2 Si + 4HCl。
Si + 4HCl。
回答下列问题:
(1)上述反应中,属于氧化还原反应的是(填序号)。
(2)反应①和③属于。
A.化合反应 B.分解反应 C.置换反应 D.复分解反应
(3)下列描述正确的是。
A.氧化还原反应都是置换反应
B.判断一个反应是否为氧化还原反应的依据是是否有化合价的升降
C.化合反应全部都是氧化还原反应
D.复分解反应全部都是氧化还原反应