一定条件下,在体积为10 L的恒容密闭容器中,发生如下反应:
2X(s)+Y(g) Z(g),经60 s达到平衡,生成0.3 mol Z,下列说法正确的是( )
Z(g),经60 s达到平衡,生成0.3 mol Z,下列说法正确的是( )
| A.用X 表示的化学反应速率为0.001 mol/(L·s) |
| B.将容器体积变为20 L,Z的平衡浓度变为原来的1/2 |
| C.若升高温度Y的转化率减小,则正反应为吸热反应 |
| D.达到平衡时,Y与Z 的浓度相等 |
下列说法可充分说明P(g)+Q(g)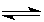 S(g)+R(g),在恒温恒容密闭容器中的反应已达平衡的是
S(g)+R(g),在恒温恒容密闭容器中的反应已达平衡的是
| A.容器里P、Q、R、S四种物质的物质的量浓度比为1:1:1:1 |
| B.单位时间内同时生成n molP和n molQ |
| C.容器内P、Q不再反应生成S和R |
| D.单位时间内同时生成n molP和n molS |
用铁片与稀硫酸反应制取氢气是,下列的措施中,不能使氢气生成速率加快的是
| A.加热 | B.不用稀硫酸,改用98﹪浓硫酸 |
| C.滴加少量硫酸铜溶液 | D.不用铁片,改用铁粉 |
.根据下表中所列键能数据,判断下列分子中,最不稳定的分子是
| 化学键 |
H—H |
H—Cl |
H—I |
Cl—Cl |
Br—Br |
| 键能/ kJ/mol |
436 |
431 |
299 |
247 |
193 |
A. B.
B.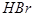 C.
C.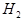 D.
D.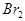
2g氢气完全燃烧生成液态水时可放出285.8KJ的热量,下列热化学方程式正确的是
| A.2H2(g)+O2(g)==2H2O(g)△H=-571.6kJ/mol |
| B.2H2(g)+O2(g)==2H2O(l)△H=-285.8kJ/mol |
| C.H2+1/2 O2==H2O△H=-285.8kJ/mol |
| D.2H2(g)+O2(g)==2H2O(l)△H=-571.6kJ/mol |
下列说法中错误的是
| A.化学反应中的能量变化通常表现为热量的变化 |
| B.化学键的断裂和形成是化学反应中能量变化的主要原因 |
| C.需要加热才能发生的反应一定是吸热反应 |
| D.反应物总能量和生成物总能量相对大小决定该反应是吸热反应还是放热反应 |