依据氧化还原反应: 2Ag+(aq) + Cu(s) ="==" Cu2+(aq) + 2Ag(s)设计的原电池如图所示。请回答下列问题:
2Ag+(aq) + Cu(s) ="==" Cu2+(aq) + 2Ag(s)设计的原电池如图所示。请回答下列问题: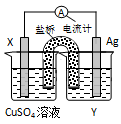
(1)电极X的材料是 ;电解质溶液Y是 。
(2)外电路中的电子是从 电极流向 电极。
(3)银电极上发生的电极反应式为
利用废铁丝和工业硫酸铜废液(含硫酸亚铁)制备硫酸铜晶体。生产过程如下: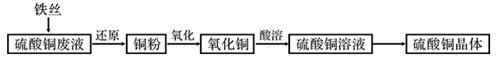
试回答下列问题:
(1)利用硫酸铜的 性质,常在游泳池中加入硫酸铜晶体杀菌消毒。
(2)废铁丝中含有铁锈((Fe2O3・xH2O))在投入硫酸铜废液前需用稀H2SO4进行处理,其主要发生反应的离子方程式_____________________。
(3)铜粉氧化过程中,颜色由粉红变为黑色,再由黑色变绿色。取绿色粉末加入稀硫酸溶液,溶液变蓝,产生无色无味气体,经检验为二氧化碳。推测该绿色粉末为 。(填化学式)
(4)为了使灼烧后的氧化铜混合物充分酸溶,在加入稀H2SO4的同时,还通入O2。通入O2的目的是(用化学反应方程式表示)____________________。
(5)硫酸铜溶液常作电解液,试写出用石墨电极电解硫酸铜溶液阳极反应式: 。
(6)在0.10mol・L-1硫酸铜溶液中加入氢氧化钠稀溶液充分搅拌有浅蓝色氢氧化铜沉淀生成,当溶液的pH=8时,c(Cu2+)=________________mol・L-1(K sp[Cu(OH)2]=2.2×10-20)。
NaNO2因外观和食盐相似,又有咸味,容易使人误食中毒。已知NaNO2能发生如下反应:2NaNO2+4HI=2NO↑+I2+2NaI+2H2O。
(1) 上述反应中氧化剂是________。
(2) 根据上述反应,鉴别NaNO2和NaCl。可选用的物质有:①碘化钾淀粉试纸、
②淀粉、③白酒、④食醋,你认为必须选用的物质有________(填序号)。
(3) 某厂废液中,含有2%~5%的NaNO2,直接排放会造成污染,下列试剂能使
NaNO2转化为不引起二次污染的N2的是________(填编号)。
| A.NaCl | B.NH4Cl |
| C.HNO3 | D.浓H2SO4 |
(4) 请配平化学方程式:□Al+□NaNO3+□NaOH=□NaAlO2+□N2↑+2H2O。
若反应过程中转移5mole-,则生成标准状况下N2的体积为_______L。
工业生产硝酸铵的流程图如下图。请回答: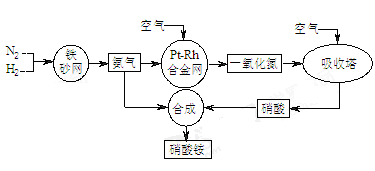
(1)已知 :N2(g)+3H2(g)  2NH3(g) ΔH=-92.4 kJ·mol-1。
2NH3(g) ΔH=-92.4 kJ·mol-1。
①在500℃、2.02×107Pa和铁催化条件下向一密闭容器中充入1molN2和3molH2,充分反应后,放出的热量_____(填“<”、“>”或“=”)92.4kJ,理由是 。
②为提高氨的产量,获得更大的效益,实际生产中宜采取的措施有 。
A 降低温度 B 最适合催化剂活性的适当高温 C 增大压强
D 降低压强 E 循环利用和不断补充氮气 F 及时移出氨
(2)已知铂铑合金网未预热也会发热。写出氨催化氧化的化学方程式: ,该反应的化学平衡常数表达式K= ,当温度升高时,K值 (填“增大”、“减小”或“不变”)。
(3)在一定温度和压强的密闭容器中,将平均相对分子质量为8.5的H2和N2混合,当该反应达到平衡时,测出平衡混合气的平均相对分子质量为10,请计算此时H2的转化率(写出计算过程)。
在一密闭容器中发生下列反应:2SO2 (g)+O2 (g) 2SO3(g) ΔH<0,如图所示是某一时间段中反应速率与反应进程的曲线关系。回答下列问题:
2SO3(g) ΔH<0,如图所示是某一时间段中反应速率与反应进程的曲线关系。回答下列问题: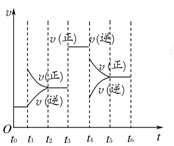
(1)处于平衡状态的时间段是____ ____。
(2)t1、t3、t4时刻,体系中分别改变的是什么条件?
t1______ __;t3______ __;t4_____ ___。
已知:①2SO2 (g)+O2 (g) 2SO3(g) ΔH=-196.6 kJ·mol-1
2SO3(g) ΔH=-196.6 kJ·mol-1
②2NO(g)+O2(g) 2NO2(g) ΔH=-113.0 kJ·mol-1
2NO2(g) ΔH=-113.0 kJ·mol-1
则反应NO2(g)+SO2(g) = SO3(g)+NO(g)的ΔH=__________kJ·mol-1。