高功率Ni/MH(M表示储氢合金)电池已经用于混合动力汽车。总反应方程式如下:
Ni(OH)2 + M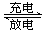 NiOOH + MH,下列叙述正确的是( )
NiOOH + MH,下列叙述正确的是( )
| A.放电时正极附近溶液的碱性增强 |
| B.放电时负极反应为:M + H2O + e-= MH + OH- |
| C.充电时阳极反应为:NiOOH + H2O + e-= Ni(OH)2 + OH- |
| D.放电时每转移1mol电子,正极有1mol NiOOH被氧化 |
分析下列反应在任何温度下均能自发进行的是
| A.2N2(g)+O2(g)===2N2O(g) ΔH=+163 kJ·mol-1 |
B.Ag(s)+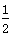 Cl2(g)===AgCl(s) ΔH=-127 kJ·mol-1 Cl2(g)===AgCl(s) ΔH=-127 kJ·mol-1 |
C.HgO(s)===Hg(l)+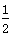 O2(g) ΔH=+91 kJ·mol-1 O2(g) ΔH=+91 kJ·mol-1 |
D.H2O2(l)=== 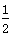 O2(g)+H2O(l) ΔH=-98 kJ·mol-1 O2(g)+H2O(l) ΔH=-98 kJ·mol-1 |
.在一定温度下的某容积不变的密闭容器中,建立下列化学平衡:C(s)+H2O(g) CO(g)+H2(g)不能确定上述可逆反应在一定条件下已达到化学平衡状态的是
CO(g)+H2(g)不能确定上述可逆反应在一定条件下已达到化学平衡状态的是
| A.体系的压强不再发生变化 |
| B.v正(CO)=v逆(H2O) |
| C.生成n mol CO的同时生成n mol H2 |
| D.1 mol H—H键断裂的同时断裂2 mol H—O键 |
、稀氨水中存在着下列平衡:NH3·H2O NH4++OH-,若要使平衡向逆反应方向移动,同时使c(OH-)增大,应加入适量的物质是
NH4++OH-,若要使平衡向逆反应方向移动,同时使c(OH-)增大,应加入适量的物质是
| A.NH4Cl | B.硫酸 | C.NaOH固体 | D.水 |
在25 ℃时,密闭容器中X、Y、Z三种气体的初始浓度和平衡浓度如下表:
| 物质 |
X |
Y |
Z |
| 初始浓度/mol·L-1 |
0.1 |
0.2 |
0 |
| 平衡浓度/mol·L-1 |
0.05 |
0.05 |
0.1 |
则25 ℃时,反应X+3Y 2Z的平衡常数为
2Z的平衡常数为
A.500B.600C.1 200D.1 600
某密闭容器中发生如下反应:X(g)+3Y(g) 2Z(g)ΔH<0如图表示该反应的速率(v)随时间(t)变化的关系,t2、t3、t5时刻外界条件有所改变,但都没有改变各物质的初始加入量。
2Z(g)ΔH<0如图表示该反应的速率(v)随时间(t)变化的关系,t2、t3、t5时刻外界条件有所改变,但都没有改变各物质的初始加入量。
下列说法中正确的是
| A.t2时加入了催化剂 | B.t3时降低了温度 |
| C.t5时增大了压强 | D.t4~t5时间内转化率最低 |