有关钴、镍和铁化合物的性质见下表:
氯化钴可用于化学反应催化剂,油漆催干剂,干湿指示剂,啤酒泡沫稳定剂,陶瓷着色剂,制造隐显墨水等。用金属钴板(含少量Fe、Ni)制备氯化钴的工艺流程如下:
钴与盐酸反应极慢,需加入催化剂硝酸才可能进行实际生产。
(1)“除镍”步骤中,NH3·H2O用量对反应收率的影响,见下表:
从表中可知x= 时,除镍效果最好。
(2)“除镍”步骤必须控制在一定的时间内完成,否则沉淀将有部分Co(OH)3生成,试写出反应的化学方程式 。
(3)“除铁”步骤中加入双氧水发生反应的离子方程式是 .
(4)“除铁”步骤中加入的纯碱作用是 。
(5)在“调pH"步骤中,加盐酸的作用是
(6)已知25℃时,Ksp[Fe(OH)3]=4.0×10-38,则该温度下反应Fe3++3H2O Fe(OH)3+3H+的平衡常数为 。
Fe(OH)3+3H+的平衡常数为 。
某工业废液里含有FeCl2、CuCl2和FeCl3。为回收铜并得到纯净的FeCl3溶液,现设计如下综合利用的主要流程。试推断:
(1)方框内物质A和B的化学式:A;B;
(2)第③步通入B的离子方程式为 ___。
氧化还原反应中实际上包含氧化和还原两个过程。下面是一个还原过程的反应式:NO3-+4H++3 e -= NO+2H2O
KMnO4、Na2CO3、FeO、Al(OH)3四种物质中的一种物质(甲)能使上述还原过程发生。
(1)写出该氧化还原反应的方程式(不需配平):
______________________________________________________;
(2)反应中,氧化剂是_________,被氧化的元素是_____________;
(3)如反应转移了0.6mol e-,则产生的气体在标准状况下体积为___ L。
人类生活离不开化学,硫酸亚铁、醋酸、小苏打、食盐、次氯酸钙、氢氧化铝都是生活中较常见的化学物质。
(1)医疗上常用_____________(从上述物质中选,填化学式)糖衣片治疗贫血病,外面包裹糖衣的目的是;
(2)治疗胃酸过多的药物主要成分是氢氧化铝或碳酸氢钠,请分别写出中和胃酸的离子方程式:____________________、 ___________________________;
(3)生活中的食醋和淀粉溶液分别属于分散系中的溶液和,用可以鉴别(填化学专用名词)。
肉桂酸是重要的有机合成中间体,广泛用于医药、香料、塑料和感光树脂等化工产品中。肉桂酸的结构简式为右图,请回答下列问题。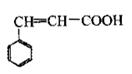
(1)肉桂酸的分子式是。
(2)写出肉桂酸的顺式结构。
(3)肉桂酸与乙醇在一定条件下发生酯化反应的化学方程式是。
(4)已知: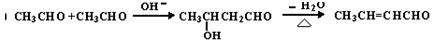
由苯甲醛制备肉桂酸的合成路线如下: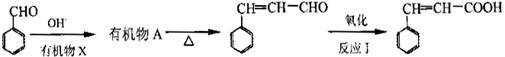
①上述合成路线中,反应I中氧化剂可选择(填写正确选项的字母)。
a.高锰酸钾酸性溶液 b.新制氧氧化铜 c.溴的四氯化碳溶液
②苯甲醛与有机物X反应生成A的化学方程式是
某有机物A由C、H、O三种元素组成,在一定条件下,A、B、C、D、E之间的转化关系如下: 170℃ O2,催化剂氧化
170℃ O2,催化剂氧化
|
浓硫酸