将10 mL淀粉胶体和5 mL氯化钠溶液混合后,放入用半透膜制成的袋内,将此袋浸入蒸馏水中(如右图所示)2 min后,分别取袋内和烧杯内液体进行实验.下列说法正确的是
| A.烧杯内液体加入硝酸银溶液后有白色沉淀产生 |
| B.烧杯内液体加入碘水后呈蓝色 |
| C.袋内液体加入硝酸银溶液后无变化 |
| D.袋内液体加入碘水后不变蓝 |
下列有关实验现象或结论的描述不正确的
| A.铅蓄电池充电时,阳极的反应为:PbSO4+2H2O+2e-=PbO2+SO42-+4H+ |
| B.FeCl2溶液与K3[Fe(CN)6]溶液混合后得到特征蓝色沉淀,利用此反应可检验Fe2+ |
| C.常温下将5mL0.1mol/LNa2S2O3溶液、5mL0.01mol/LNa2S2O3溶液分别与5mL0.1mol/LH2SO4溶液混合并搅拌,通过记录溶液中出现浑浊的时间,可确定浓度对化学反应速率的影响 |
| D.处理含有Hg2+离子的废水可加入硫化钠,使Hg2+离子转化为HgS沉淀 |
现有常温下的四份溶液: ① 0.01 mol/L CH3COOH ② 0.01 mol/LHCl ③pH=12的氨水 ④ pH=12的NaOH溶液,下列说法正确的是
| A.①中水的电离程度最小,③中水的电离程度最大 |
| B.将四份溶液稀释相同倍数后,溶液的pH:②﹥①,③﹥④ |
| C.将②③混合,若pH=7,则消耗溶液的体积:②﹥③ |
| D.将①、④混合,若有c(CH3COO-)﹥c(H+),则混合液一定呈碱性 |
一定条件下,在密闭容器里进行如下可逆反应:S2Cl2(橙黄色液体)+Cl2(气) 2SCl2(鲜红色液体) ΔH=-61.16 kJ·mol-1。下列说法正确的是
2SCl2(鲜红色液体) ΔH=-61.16 kJ·mol-1。下列说法正确的是
| A.增大压强,平衡常数将增大 |
| B.达到平衡时,单位时间里消耗n mol S2Cl2的同时也生成n molCl2 |
| C.达到平衡时,若升高温度,氯气的百分含量减小 |
| D.加入氯气,平衡向正反应方向移动,氯气的转化率一定升高 |
某溶液可能含有Cl-、SO42-、CO32-、NH4+、Fe3+、Al3+和K+。取该溶液100 mL,加入过量NaOH溶液,加热,得到0.02 mol气体,同时产生红褐色沉淀;过滤,洗涤,灼烧,得到1.6 g固体;向上述滤液中加足量BaCl2溶液,得到4.66 g不溶于盐酸的沉淀。由此可知原溶液中
| A.至少存在5种离子 |
| B.CO32-、Al3+一定不存在,K+可能存在 |
| C.SO42-、NH4+一定存在,Cl-可能不存在 |
| D.Cl-一定存在,且c(Cl-)≥0.4 mol·L-1 |
某研究小组利用“钯催化交叉偶联反应”合成了有机物丙,合成路线如下: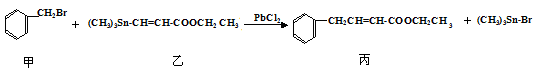
下列分析判断正确的是
| A.分离提纯有机物丙宜在NaOH热溶液中进行 |
| B.PbCl2的作用是提高反应物的活性,加快反应速率 |
| C.可用酸性KMnO4溶液检验有机物丙中是否含有机物乙 |
| D.利用NaOH溶液、AgNO3溶液即可确定有机物甲中含有溴元素 |