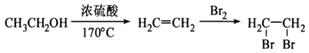(10分)(1)已知下列变化过程中,0.2 mol R2O72-与0.2 mol K2SO3恰好反应,则R被还原的价态为____。
(2)在100 mL 0.100 mol·L-1的FeBr2溶液中通入Cl2,若要使Fe2+刚好反应完全,则需标准状况下C l2________ mL。
l2________ mL。
(3)某反应中反应物与生成物有:AsH3、H2SO4、KBrO3、K2SO4、H3AsO4、H2O和一种未知物质X.
①已知KBrO3在反应中得到电子,则该反应的还原剂是______________________.
②已知0.2 mol KBrO3在反应中得到1mol电子生成X,则X的化学式为______________.
mol KBrO3在反应中得到1mol电子生成X,则X的化学式为______________.
Ⅰ某温度下,密闭容器中充入1 mol N2和3 mol H2,使之反应合成NH3,平衡后,测得NH3的体积分数为w,如果温度不变,只改变起始加入量,使之反应平衡后NH3的体积分数仍为w,N2、H2、NH3的物质的量分别用x、y、z表示.
(1)恒温恒容条件下:若x=0.75 mol, 则y=________,z=________.
(2)恒温恒压条件下,x、y、z(均不小于0)满足的一般条件是_______________________.
Ⅱ一定条件下,可逆反应X(g)+Y(g) 2Z(g)达到平衡时,各物质的平衡浓度为c(X)=0.5mol/L;c(Y) ="0.1" mol /L ; c (Z)="1.6" mol /L若用a、b、c 分别表示X Y Z的初始浓度(mol/L)则a、b应满足的关系是____________, a的取值范围为_______________
2Z(g)达到平衡时,各物质的平衡浓度为c(X)=0.5mol/L;c(Y) ="0.1" mol /L ; c (Z)="1.6" mol /L若用a、b、c 分别表示X Y Z的初始浓度(mol/L)则a、b应满足的关系是____________, a的取值范围为_______________
Ⅲ在10℃和4×105Pa的条件下,当反应aA(g) dD(g)+eE(g),建立平衡后,维持温度不变而压强改变,测得D的浓度变化如下:
dD(g)+eE(g),建立平衡后,维持温度不变而压强改变,测得D的浓度变化如下:
| 压强(Pa) |
4×105 |
6×105 |
10×105 |
20×105 |
| D的浓度(mol/L) |
0.085 |
0.126 |
0.200 |
0.440 |
(1)压强从4×105Pa增加到6×105Pa时,平衡向(填“正”或“逆”)方向移动,理由是_________________________________________________________________
(2)压强从10×105Pa增加到20×105Pa时,平衡向_______(填“正”或“逆”)方向移动
有铜片、锌片和250mL稀硫酸组成的原电池,当在铜片上放出4.48L(标准状况下)的气体时,硫酸恰好完全反应。
(1)该原电池的正极反应式
(2) 原稀硫酸的物质的量浓度是 mol/ L
(3)锌片减少的质量
现有10种元素的性质、数据如下表所列,它们均为短周期元素。
| A |
B |
C |
D |
E |
F |
G |
H |
I |
J |
|
| 原子半径(10-10m) |
0.74 |
1.60 |
1.52 |
1.10 |
0.99 |
1.86 |
0.75 |
0.82 |
0.102 |
0.037 |
| 最高或最低 化合价 |
+2 |
+1 |
+5 |
+7 |
+1 |
+5 |
+3 |
+6 |
+1 |
|
| -2 |
-3 |
-1 |
-3 |
-2 |
回答下列问题:
(1)D的元素名称是,
H的元素符号是。
B在元素周期表中的位置是(周期、族)
(2)在以上元素形成的最高价氧化物的水化物中,酸性最强的化合物的分子式是。
化合物F2A2的电子式是:,构成该物质的化学键类型为________________
(3)用电子式表示A的简单氢化物的形成过程如下:;
G的氢化物的结构式为。
(4)一定条件下,IA2气体与足量的A单质充分反应生成20g气态化合物,放出24.6 kJ热量,写出其热化学方程式。
(5)用J元素的单质与A元素的单质可以制成电池,电池中装有KOH浓溶液,用多孔的惰性电极甲和乙浸入KOH溶液,在甲极通入J的单质,乙极通入A的单质,则甲极的电极反应式为:____________________。
(10分)通常人们把拆开1mol 某化学键所吸收的能量看成该化学键的键能。键能的大小可用于估算化学反应的反应热(△H)。
| 化学键 |
Cl-Cl |
H—H |
H—Cl |
N≡N |
| 键能/kJ·mol |
243 |
436 |
431 |
946 |
(1)按要求完成填空
a 2HCl(g) = H2(g)+Cl2(g);△H=
bN2 (g)+3H2(g)= 2NH3(g) ΔH="-92" kJ/mol,则N—H键的键能是kJ·mol
(2)1 mol NO2和1mol CO反应生成CO2和NO过程中能量变化示意图,请写出NO2和CO反应的热化学方程式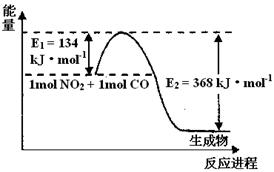
(3)已知在常温常压下:
① 2CH3OH(l) + 3O2(g) = 2CO2(g) + 4H2O(g)ΔH1
② 2CO (g)+ O2(g) = 2CO2(g)ΔH2
③ H2O(g) = H2O(l)ΔH3
则CH3OH(l)+O2(g)=" CO(g)" + 2H2O(l)ΔH=(用含ΔH1、ΔH2、ΔH3的式子表示)
(4)已知:2Al (s)+ 3/2O2(g)==Al2O3(s)△H=" -1" 644.3 kJ• mol-1
2Fe (s) +3/2O2(g)==Fe2O3(s)△H=" -815.88" kJ• mol-1
试写出铝粉与氧化铁粉末发生铝热反应的热化学方程式_______________________。
相对分子质量为92的某芳香烃X是一种重要的有机化工原料,研究部门以它为初始原料设计出如下转化关系图(部分产物、合成路线、反应条件略去)。其中A是一氯代物,H是一种功能高分子,链节组成为C7H5NO。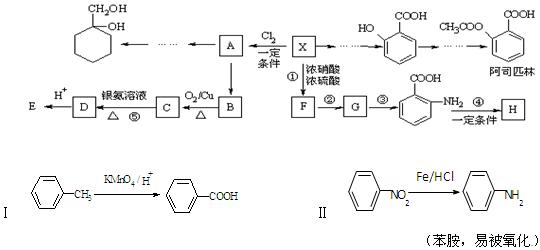
请根据所学知识与本题所给信息回答下列问题:
⑴ H的结构简式是;
⑵反应②、③的类型分别是,。
⑶反应⑤的化学方程式是;
⑷阿司匹林最多消耗mol NaOH;
⑸ 有多种同分异构体,其中含有1个醛基和2个羟基的芳香族化合物共有种;
有多种同分异构体,其中含有1个醛基和2个羟基的芳香族化合物共有种;
⑹请用合成反应流程图表示出由A和其他无机物合成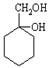 最合理的方案(不超过4步)。
最合理的方案(不超过4步)。
流程图示例: