某无色溶液中含有CO32-、K+、NH4+、Ba2+、SO42-、Fe3+中几种离子,今取二份体积各100mL该溶液进行实验。
(1)第一份加入足量氢氧化钠浓溶液,加热,产生的氨气在标准状况下体积为896mL;
(2)第二份加入足量氯化钡溶液,生成沉淀质量为6.27g,再经足量稀盐酸洗涤后得2.33g残渣。
据此回答:
①用稀盐酸洗涤沉淀时反应的离子方程式为 ;
②含有的阴离子及其对应物质的量浓度依次是 ;
③对是否存在K+的判断依据是 。
8分)某有机物的结构简式为 HOCH2 CH=CHCOOH,
(1)写出该有机物中所含的官能团的名称________________________________
(2)写出该有机物与溴水反应的化学方程式________________________________
(3)写出该有机物与足量NaHCO3溶液反应的化学方程式_____________________
(4)写出该有机物与乙酸反应的化学方程式________________________________
(9分)在2L密闭容器内,800℃时反应:2NO(g)+O2(g) 2NO2(g)体系中,n(NO)随时间的变化如表:
2NO2(g)体系中,n(NO)随时间的变化如表:
| 时间(s) |
0 |
1 |
2 |
3 |
4 |
5 |
| n(NO)(mol) |
0.020 |
0.010. |
0.008 |
0.007 |
0. 007 |
0.007 |
⑴NO的平衡转化率为_______
⑵下图中表示NO2的浓度变化曲线是。
用O2表示从0~2s内该反应的平均速率v=。
⑶能说明该反应已达到平衡状态的是。
a.v (NO2)="2" v (O2) b.容器内压强保持不变
c.v逆(NO)="2" v正 (O2) d.容器内混合气体的密度保持不变
e.该容器内颜色保持不变
(10分)短周期元素A、B、C、D中,0.5mol A元素的离子得到6.02×1023个电子被还原为中性原子,0.4g A的氧化物恰好与100ml 0.2mol/L的盐酸完全反应,A原子核内质子数目与中子数目相等,B元素原子核外第三层电子数目比第一层多1个,C—比A元素的离子多1个电子层,D元素的原子核外第二层比第一层多2个电子。回答下列问题:
(1)C―的结构示意图为;
与C同族的上一周期元素的气态氢化物的稳定性比HC的________(填“强”或“弱”);
与C同族的上一周期元素的气态氢化物的沸点比HC的________(填“高”或“低”);
(2)元素D的最高价氧化物的电子式为_______,D的气态氢化物的二氯代物有_____种结构。
(3)工业上冶炼单质A的化学方程式为_____________________________________;
(4)若将单质A、B用导线连接插入到氢氧化钠溶液中可以组成原电池,则正极材料是_______(用化学式填写),负极电极反应是___________________________________。
已知:
I.冠心平F是降血脂、降胆固醇的药物,它的一条合成路线如下:
(1)A为饱和一元羧酸,8.8g A与足量NaHCO3溶液反应生成2.24L CO2(标准状况),A的分子式为___________________。
(2)写出符合A分子式的所有甲酸酯的结构简式: ______________________________。
(3)B是氯代羧酸,其核磁共振氢谱有两个峰,写出B→C的反应方程式:
__________________________________________________________。
(4)C+E→F的反应类型为________________________。
(5)写出A和F的结构简式:A______________________; F__________________________。
(6)D的苯环上有两种氢,它所含官能团的名称为___________________;写出a、b所代表的试剂:a ______________; b___________。
Ⅱ. 按如下路线,由C可合成高聚物H:
(7)C G的反应类型为_____________________.
G的反应类型为_____________________.
(8)写出G H的反应方程式:_______________________。
H的反应方程式:_______________________。
实验室用加热l-丁醇、溴化钠和浓H2SO4的混合物的方法来制备1-溴丁烷时,还会有烯、醚等副产物生成。反应结束后将反应混合物蒸馏,分离得到1—溴丁烷,已知相关有机物的性质如下: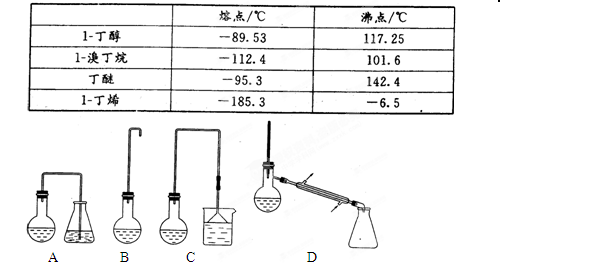 ⑴反应中由于发生副反应而生成副产物的有机反应类型有_________________。
⑴反应中由于发生副反应而生成副产物的有机反应类型有_________________。
⑵制备1-溴丁烷的装置应选用上图中的_______(填序号)。反应加热时的温度不宜超过100℃,理由是__________________________;较好的加热方法是_____________。
⑶当给烧瓶中的混合物加热时,溶液会出现橘红色,其原因是_____________。
⑷反应结束后,将反应混合物中1-溴丁烷分离出来,应选用上图的装置是______。该操作应控制的温度(t)范围是_______________。