用已知浓度的盐酸滴定未知浓度的NaOH溶液时,下列操作导致结果偏大的是( )
| A.碱式滴定管用蒸馏水洗净后,直接加入未知浓度的NaOH溶液 |
| B.锥形瓶用蒸馏水洗净后,直接加入一定体积的未知浓度的NaOH溶液 |
| C.滴定前,没有逐出酸式滴定管尖嘴处的气泡,滴定终点时气泡消失 |
| D.滴定前读数正确,达到滴定终点后,俯视读数 |
查处酒后驾驶采用的“便携式乙醇测量仪”以燃料电池为工作原理,在酸 性环境中,理论上乙醇可以被完全氧化为CO2,但实际乙醇被氧化为X,其中一个电极的反应式为:CH3CH2OH-2e-→X+2H+。下列说法中正确的是
性环境中,理论上乙醇可以被完全氧化为CO2,但实际乙醇被氧化为X,其中一个电极的反应式为:CH3CH2OH-2e-→X+2H+。下列说法中正确的是
| A.电池内部H+由正极向负极移动 |
| B.另一极的电极反应式为:O2 + 4e- + 2H2O = 4OH- |
| C.乙醇在正极发生反应,电子经过外电路流向负极 |
D.电池总反应为:2CH3CH2OH+O2→ 2CH3CHO+2H2O 2CH3CHO+2H2O |
在合成氨反应中,经过5秒钟,NH3的浓度增加了1.5mol·L-1,在这5秒钟内,下列平均 反应速率正确的是
反应速率正确的是
① v(NH3)=0.15 mol·L-1·s-1② v(H2)=0.45 mol·L-1·s-1
③ v(N2)=0.15 mol·L-1·s-1④ v(H2)=0.3mol·L-1·s-1
| A.①② | B.②③ | C.③④ | D.①④ |
将纯锌片和纯铜片按图示方式插入同浓度的稀硫酸中一段时间,以下叙述正确的是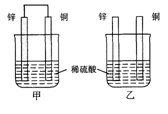
| A.两烧杯中铜片表面均无气泡产生 |
| B.甲中铜片是正极,乙中铜片是负极 |
| C.两烧杯中溶液的pH均增大 |
| D.产生气泡的速度甲比乙慢 |
胶状液氢(主要成分是H2和CH4)有望用于未来的运载火箭和空间运输系统。实验测得:101kPa时,1mol H2完全燃烧生成液态水,放出285.8 kJ的热量;1 mol CH4完全燃烧生成液态水和CO2,放出890.3kJ的热量。下列热化学方程式书写正确的是
kJ的热量;1 mol CH4完全燃烧生成液态水和CO2,放出890.3kJ的热量。下列热化学方程式书写正确的是
| A.CH4(g)+2O2(g)=CO2(g)+2H2O(g);△H=-890.3kJ·mol—1 |
| B.1/2CH4(g)+O2(g)=1/2CO2(g)+H2O(l);△H=-445.15kJ·mol—1 |
| C.CH4(g)+2O2(g)=CO2(g)+2H2O(l);△H=-890.3kJ |
| D.2H2(g)+O2(g)=2H2O(l);△H=-285.8kJ·mol—1 |
下列变化属于吸热反应的是
①液态水气化②将胆矾加热变为白色粉末③浓硫酸稀释④氯酸钾分解制氧气 ⑤生石灰与水反应生成熟石灰⑥水煤气反应⑦二氧化碳与赤热的炭反应生成一氧化碳
⑤生石灰与水反应生成熟石灰⑥水煤气反应⑦二氧化碳与赤热的炭反应生成一氧化碳
| A.①④⑤⑦ | B.②③⑥ | C.①②④⑦ | D.②④⑥⑦ |