(10分)含有弱酸HA和其钠盐NaA的混合溶液,在化学上用作缓冲溶液。向其中加入少量酸或碱时,溶液的酸碱性变化不大。 (1)向该溶液中加入少量盐酸时,发生反应的离子方程式是 ,
(1)向该溶液中加入少量盐酸时,发生反应的离子方程式是 ,
向其中加入少量KOH溶液时,发生反应的离子方程式是 ;
(2)现将0.04 mol·L-1HA溶液和0.02 mol·L-1NaOH溶液等体积混合,得到缓冲溶液。
①若HA为HCN,该溶液显碱性,则溶液 中c(
中c( Na+) c(CN-)(填“<”、“=”或“>”),你得出该结论的依据是 ;
Na+) c(CN-)(填“<”、“=”或“>”),你得出该结论的依据是 ;
②若HA为CH3COOH,该溶液显酸性。溶液中所有的离子按浓度由大到小排列的顺序是 。
(共10分)A、B、C、D、E、F、G是中学里常遇到的一些物质,它们之间有如下转化关系,有些必要的信息已在框图中注明:
回答下列问题:
(1)D的空间构型为,C的电子式为,F溶液名称是,
(2)在实验室中制取气体A的离子方程式是.
(3)写出A+D→C的化学方程式 ,
氧化剂与还原剂物质的量之比为,
(4)写出:F+B(过量)→E的离子方程式 ,
(共7分)(1)在热的稀硫酸溶液中溶解了11.4gFeSO4.当加入50mL0.5mol/LKNO3
溶液后,使其中的Fe2+全部转化成Fe3+,KNO3也反应完全,并有NxOy氮氧化物气体逸出.
□FeSO4+□KNO3+□H2SO4→□K2SO4+□Fe2(SO4)3+□NXOy+□H2O
①推算出x=________,y=________.
②配平该化学方程式(系数填写在上式方框内)
③反应中氧化剂为________.
④用短线和箭头标出电子转移的方向和总数.
晶体具有规则的几何外形,晶体中最基本的重复单位称晶胞。氯化钠晶体结构如图所示,已知NixO晶体晶胞结构为氯化钠型,由于晶体缺陷,x值小于1,测知NixO晶体的密度为7.4g/cm3,晶胞边长为4.0×10-10m(NA用6.0x1023计算)。试回答(要求计算过程):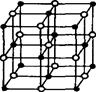
(1)NixO晶体中的x值_________(精确到0.01)。
(2)晶体中的Ni分别为Ni2+、Ni3+,此晶体化学式____________(用含Ni2+、Ni3+表示)。
将2mol X和1mol Y的混合气体置于等压密闭容器中,此时容器的体积为120 L,在一定温度下发生反应:2X(g)+Y(g) 2Z(g)。当反应达到平衡状态A时,测得气体的密度变为反应前的1.2倍。请回答下列问题:
2Z(g)。当反应达到平衡状态A时,测得气体的密度变为反应前的1.2倍。请回答下列问题:
(1)达平衡状态A时,Y的转化率为________,容器的体积为_________;在达到平衡状态A的容器中通人少量Y,体系中X的体积分数将_______(填“增大”或“减小”或“不变”)。
(2)若在同一容器中起始加入X、Y、Z分别为a、b、c mol,达到 平衡后Y的体积分数与平衡状态A相同,则起始时a、b、c应满足的关系为___________.___________。
平衡后Y的体积分数与平衡状态A相同,则起始时a、b、c应满足的关系为___________.___________。
(3)若反应在一体积为120 L的等容密闭容器中进行,要使平衡后各气体体积分数与平衡状态A相同,则起始时应加入X:_________mol,Y:_________mol,Z:0 mol。
有关元素A.B.C.D的信息如下:
| 元素 |
有关信息 |
| A |
最高价氧化物对应的水化物(甲)能与其气态氢化物(乙)反应生成盐 |
| B |
地壳中含量最高的元素,A与B可形成一种质量比为 7︰12的化合物(丙) |
| C |
单质曾用于焊接钢轨 |
| D |
单质是生活中常见金属,其制品在自然环境中被腐蚀呈现红棕色 |
请回答下列问题:
(1)乙分子的空间构型________,用电子式表示乙的形成过程____________________。
(2)有关C与D元素,下列说法正确的是____________________ (填序号)。
① C或D的高价盐均可用做净水剂
②用C或D单质做成的槽车,都可用来运输甲的稀溶液
③ C、D的单质与稀硫酸组成的原电池,C电极发生氧化反应
④ C的合金可用来做车船材料和门窗等
(3)B的一种氢化物在碱性溶液中可与丙反应,生成物中A元素只显其最高价态,该反应的离子方程式是________________________________________。
(4)现取1 mol/L 100 mL的C的氯化物溶液,向其中加入1 mol/L氢氧化钠溶液产生了3.9 g的沉淀,则加入的氢氧化钠溶液体积 可能是____________________mL。
可能是____________________mL。
(5)已知:2AB2(g) A2B4(g);△H<0。在恒温恒容条件下,将一定量AB2和A2B4的混合气体通入容积为2L的密闭容器中,反应过程中各物质的物质的量浓度c随时间t的变化关系如下图所示。
A2B4(g);△H<0。在恒温恒容条件下,将一定量AB2和A2B4的混合气体通入容积为2L的密闭容器中,反应过程中各物质的物质的量浓度c随时间t的变化关系如下图所示。
 ① a、b、c、d四个点中,化学反应处于平衡状态的是_______点。
① a、b、c、d四个点中,化学反应处于平衡状态的是_______点。
② 25 min时,增加了_______(填物质的化学式)________mol。
③ a、b、c、d四个点所表示的反应体系中,气体颜色由深到浅的顺序是_______(填字母)。