(每空2分,共8分)
(1) 除去NaHCO3溶液中混有的Na2CO3,相应的化学方程式_____________。
(2) 除去Na2CO3固体中混有的NaHCO3,相应的化学方程式_____________。
(3) 除去CO2气体中混有的HCl,相应的离子方程式___________________。
(4) 除去Fe2O3中混有的Al2O3,相应的离子方程式_____________________。
下图为元素周期表的一部分,根据元素①~⑧在周期表中的位置,按要求回答下列问题。
| 族 周期 |
IA |
0 |
||||||
| 1 |
① |
IIA |
IIIA |
ⅣA |
VA |
ⅥA |
VIIA |
|
| 2 |
② |
③ |
||||||
| 3 |
④ |
⑤ |
⑥ |
⑦ |
⑧ |
(1)在元素①~⑧中,金属性最强的元素是_____________(填元素符号),最不容易形成化合物的元素是______________(填元素符号)。
(2)用电子式表示⑦的气态氢化物的形成过程__________________________________。
(3)③、④、⑥中原子半径由大到小的顺序是____________________(填元素符号)。
(4)表中两种元素的原子按1:1组成的常见液态化合物X易被催化分解。某同学取5支大小相同的试管,各加入等物质的量浓度等体积的X溶液,分别进行下列实验,研究外界条件对X分解反应速率的影响,实验记录如下表所示。
| 序号 |
条件 |
现象 |
结论 |
||
| 温度/℃ |
催化剂 |
||||
| 第一组 |
1 |
40 |
FeCl3溶液 |
快速产生大量气泡 |
相同条件下,温度升高,化学反应速率加快 |
| 2 |
20 |
A |
缓慢产生适量气泡 |
||
| 3 |
5 |
FeCl3溶液 |
缓慢产生极少量气泡 |
||
| 第二组 |
4 |
t |
MnO2 |
快速产生大量气泡 |
|
| 5 |
20 |
无 |
缓慢产生极少量气泡 |
①第一组实验目的是:相同条件下,探究________________对该反应速率的影响。
实验2的催化剂A是___________________。
②第二组实验中,实验4的温度t是_________________,发生反应的化学方程式是___________________________________________________________________________。
第二组实验结论是:__________________________________________________。
乙烯的产量通常用来衡量一个国家的石油化工水平。以乙烯为主要原料合成重要的有机化合物路线如下图所示。请回答下列问题。
(1)乙烯的结构简式___________,电子式_______________。
(2)A物质所含官能团的名称是__________________。
(3)反应②的反应类型是_______________________。
(4)反应③的化学方程式是___________________________________。
(5)以乙烯为原料可合成有机高分子化合物D,反应①的化学方程式是
____________________________________________________________。
(6)下列物质中,可以通过乙烯加成反应得到的是_____(填序号)。
a. CH3CH3 b. CH3CHCl2 c. CH3CH2Br
能源是现代社会发展的支柱之一。
(1)化学反应中的能量变化,通常主要表现为热量的变化。
①下列反应中,属于放热反应的是___________(填序号)。
a. Ba(OH)2·8H2O与NH4Cl混合搅拌
b. 高温煅烧石灰石
c. 铝与盐酸反应
②某同学进行如下图所示实验,测量稀盐酸与烧碱溶液中和反应的能量变化。实验表明:反应温度升高,由此判断该反应是_______(填“吸热”或“放热”)反应,其离子方程式是_______________。
(2)电能是现代社会应用最广泛的能源之一。
下图所示的原电池装置中,其负极是_____________________,正极上能够观察到的现象是____________________________,正极的电极反应式是_________________________。
原电池工作一段时间后,若消耗锌6.5g,则放出气体__________g。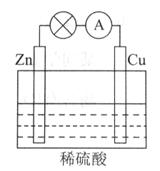
下列各组物质
①CH4和C3H8 ②醋酸和乙酸
③CH3CH2CH2CH3和 ④氕、氘、氚
④氕、氘、氚
请将正确的序号填在横线上:
属于同种物质的是__________________;互为同位素的是_________________;
互为同系物的是_____________________;互为同分异构体的是_______________。
工业废水中常含有一定量的Cr2O72-和CrO42-,它们会对人类及生态系统产生很大损害,必须进行处理。常用的处理方法有两种。
方法1:还原沉淀法。该法的工艺流程为CrO42- Cr2O72-
Cr2O72- Cr3+
Cr3+ Cr(OH)3↓
Cr(OH)3↓
其中第①步存在平衡:2CrO42- (黄色)+2H+ Cr2O72- (橙色)+H2O
Cr2O72- (橙色)+H2O
(1)若平衡体系的pH=2,该溶液显________色。
(2)能说明第①步反应达平衡状态的是__________。
a.Cr2O72-和CrO42-的浓度相同
b.2v(Cr2O72-)=v(CrO42-)
c.溶液的颜色不变
(3)第②步中,还原1 mol Cr2O72-离子,需要________mol的FeSO4·7H2O。
(4)第③步生成的Cr(OH)3在溶液中存在以下沉淀溶解平衡:Cr(OH)3(s)  Cr3+(aq)+3OH-(aq),常温下,Cr(OH)3的溶度积Ksp=c(Cr3+)·c3(OH-)=10-32,要使c(Cr3+)降至10-5mol/L,溶液的pH应调至_______。
Cr3+(aq)+3OH-(aq),常温下,Cr(OH)3的溶度积Ksp=c(Cr3+)·c3(OH-)=10-32,要使c(Cr3+)降至10-5mol/L,溶液的pH应调至_______。
方法2:电解法。该法用Fe做电极电解含Cr2O72-的酸性废水,随着电解进行,在阴极附近溶液pH升高,产生Cr(OH)3沉淀。
(5)用Fe做电极的原因为__________________。
(6)在阴极附近溶液pH升高的原因是(用电极反应解释)_________________________________。溶液中同时生成的沉淀还有__________。