下图为元素周期表的一部分,根据元素①~⑧在周期表中的位置,按要求回答下列问题。
| 族 周期 |
IA |
|
0 |
|||||
| 1 |
① |
IIA |
IIIA |
ⅣA |
VA |
ⅥA |
VIIA |
|
| 2 |
|
|
|
|
|
② |
③ |
|
| 3 |
④ |
⑤ |
|
|
|
⑥ |
⑦ |
⑧ |
(1)在元素①~⑧中,金属性最强的元素是_____________(填元素符号),最不容易形成化合物的元素是______________(填元素符号)。
(2)用电子式表示⑦的气态氢化物的形成过程__________________________________。
(3)③、④、⑥中原子半径由大到小的顺序是____________________(填元素符号)。
(4)表中两种元素的原子按1:1组成的常见液态化合物X易被催化分解。某同学取5支大小相同的试管,各加入等物质的量浓度等体积的X溶液,分别进行下列实验,研究外界条件对X分解反应速率的影响,实验记录如下表所示。
| |
序号 |
条件 |
现象 |
结论 |
|
| 温度/℃ |
催化剂 |
||||
| 第一组 |
1 |
40 |
FeCl3溶液 |
快速产生大量气泡 |
相同条件下,温度升高,化学反应速率加快 |
| 2 |
20 |
A |
缓慢产生适量气泡 |
||
| 3 |
5 |
FeCl3溶液 |
缓慢产生极少量气泡 |
||
| 第二组 |
4 |
t |
MnO2 |
快速产生大量气泡 |
|
| 5 |
20 |
无 |
缓慢产生极少量气泡 |
①第一组实验目的是:相同条件下,探究________________对该反应速率的影响。
实验2的催化剂A是___________________。
②第二组实验中,实验4的温度t是_________________,发生反应的化学方程式是___________________________________________________________________________。
第二组实验结论是:__________________________________________________。
ZnO具有抗菌性,也是重要的轮胎添加剂。工业上由粗ZnO(含FeO、CuO)制备活性ZnO流程如下: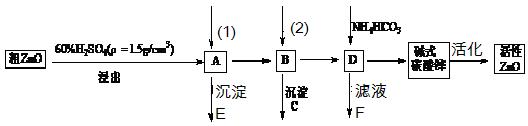
已知此溶液中Fe2+、 Fe3+、 Cu2+、 Zn2+形成氢氧化物的pH如下表
| 离子 |
开始沉沉淀的pH |
完全沉淀的pH |
| Fe2+ |
6.4 |
8.4 |
| Fe3+ |
2.4 |
3.1 |
| Cu2+ |
5.2 |
6.5 |
| Zn2+ |
6.8 |
9 |
(1)已知H2O2酸性溶液中能氧化Fe2+,反应的离子方程式为
(2)题目中框图中的(1)和(2)是需要加入的试剂依次是_______、_______。(用序号回答)
①ZnO②H2O2较浓溶液③Na2CO3溶液
(3)加入试剂(2)应将杂质离子完全转化成沉淀C, 溶液的pH应控制在;
要实现该步骤中pH的控制,应使用来检查溶液的pH
(4)书写碱式碳酸锌焙烧制备活性ZnO的化学方程式.
(5)重晶石(主要成分BaSO4)是制备钡的化合物的重要原料,但BaSO4不溶于酸,工业上常常将其转化为BaCO3,再进一步制备其他钡的化合物。已知Ksp(BaSO4) = 1.0×10-10,Ksp(BaCO3) = 2×10-9。计算将BaSO4(s)转化为BaCO3(s)所需C(CO32-)应mol/L
传统制取甲醇的原理是CO(g)+ 2H2(g) CH3OH(g) ---------①
CH3OH(g) ---------①
25℃时,K=2.68×1022
最近科学家提出“绿色自由”构想:把空气吹入碳酸钾溶液,然后再把CO2从溶液中提取出来,经化学反应后使空气中的CO2转变为可再生燃料甲醇。“绿色自由”构想技术流程如下: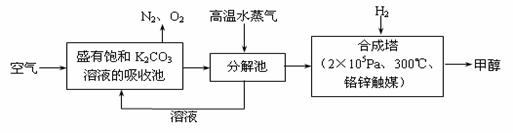
 反应原理为①CO2(g)+3H2(g) CH3OH(g)+H2O(g)------------------②
反应原理为①CO2(g)+3H2(g) CH3OH(g)+H2O(g)------------------②
25℃时,K=3.96×1011
回答:
(1)相同条件下,反应①与反应②相比,转化率更大的是,(用①②回答)
(2)写出反应②的平衡常数表达式K=,
(3)在30MPa压强下,测得反应②的实验数据如下表。分析表中数据回答下列问题:
 |
500 |
600 |
700 |
800 |
| 1.5 |
45 |
33 |
20 |
12 |
| 2.0 |
60 |
43 |
28 |
15 |
| 3.0 |
83 |
62 |
37 |
22 |
温度升高,K值(填“增大”、“减小”、或“不变”)。反应的△H0(填>、=、<)
(4)下列措施中能使n(CH3OH)/n(CO2)增大的是___________。(设合成塔为密闭容器)
| A.升高温度 | B.充入He(g) |
| C.将H2O(g)从体系中分离 | D.再充入1mol CO2和3mol H2 |
(5)甲醇可制作燃料电池。写出以氢氧化钾为电解质的甲醇燃料电池负极反应式。
(10分)
Ⅰ、A物质的化学式为M(OH)2,将其溶于水制成稀溶液,该溶液呈中性,在溶液中存在:
M2+ + 2OH- M(OH)2
M(OH)2 2H+ + MO22-
2H+ + MO22-
回答以下题目一律用“增大”“减小”“不变”填空
(1)在其他条件不变的情况下,25Co时,在蒸馏水中加入A物质后,与加入前比较,
①由水电离出的C(OH-),C(H+),水的电离度,Kw
(2)25Co时,向A的稀溶液中加入少量的烧碱固体。
则水的电离度,溶液的pH
Ⅱ、.(2分)室温下,甲、乙两瓶氨水的浓度分别为1mol/L和0.1mol/L,则甲、乙两瓶氨水中C(OH-)之比为10 (填大于、等于或小于)
下图中A、B、C、D、E均为有机化合物。已知:C能跟NaHCO3(发生反应,C和D的相对分子质量相等,且E为无支链的化合物。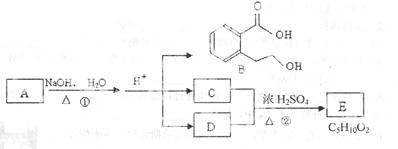
根据上图回答问题:
(l) C分子中的官能团名称是_______;化合物B不_发生的反应是_______(填字母序号):
a、加成反应b、取代反应C、消去反应d、酯化反应e、水解反应f、置换反应
(2) 反应②的化学方程式是______________。
(3) 试分析反应②加热的原因。
I、___________________________________。
II 、___________________________________
(4) A的结构简式是_____________________。
(5) 同时符合下列三个条件的B的同分异构体的数目有_______个。
I.间二取代苯环结构;II.属于非芳香酸酯;III-与FeCl3溶液发生显色反应。
写出其中任意一个同分异构体的结构简式_____________________。
(6) 常温下,将C溶液和NaOH溶液等体积混合,两种溶液的浓度和混合后所得溶液的pH如下表:
从m组情况分析,所得混合溶液中由水电离出的c(OH )=_______mol.L-1.
n组混合溶液中离子浓度由大到小的顺序是______________。
室温下,将一定浓度的Na2CO3溶液滴入CnSO4溶液中得到了蓝色沉淀。为了确定沉淀的组成,某研究性学习小组进行了以下试验和研究。
(一)【提出假说】
假设一:两者反应只生成CuCO3—种沉淀;
假设二:这两者祁互促进水解,生成Cu(OH)2—种沉淀,则此反应化学方程式为:____________________________;
假设三:生成的是CuCO3和Cu(OH)2两种沉淀。
(二)【理论探究】
查阅资料:CuCO3, Cu(OH)2均不带结晶水;
Cu(OH)2均不带结晶水;
 ;若由此数据判断,假设_______是不正确的。
;若由此数据判断,假设_______是不正确的。
(三)[实验探究]
步滋一:将CuCO4溶液倒入等浓度等体积的Na2CO3溶液中并搅拌,有蓝色沉淀生成。
步骤二:将沉淀从溶液中分离出来,其操作方法为:①过滤,②_______,③干燥。
步骤三:利用下图所示装置,进行定量分析: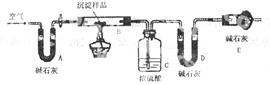
①仪器组装好后首先要进行的实验操作是_____________________。
②实验结束时通入过量空气的作用是_____________________。
③数据记录和分析:实验过程中测定的数据有:W1——样品的质量;W2——反应后装置B中残渣的质量;W3——反应生成的水的质量;W4——反应后生成二氧化碳的质量,为了测定其组成,至少需要其中 个数据,请将可能的组合填入下表中(每个空格中填一种组合,有几种组合就填几种,不必填满.)