(1)①根据图示,写出反应的热化学方程式: 。
②根据如图所示情况,判断下列说法中正确的是( )
| A.其热化学方程式为:CO(g)+H2O(g)===CO2(g)+H2(g) ΔH=+41 kJ/mol |
| B.该反应为吸热反应 |
| C.该反应为放热反应 |
| D.当H2O为液态时,其反应热值小于41 kJ/mol |
(2)已知16 g固体硫完全燃烧时放出148.4 kJ的热量,该反应的热化学方程式是 。
(3)如图是某温度下,N2与H2反应过程中能量变化的曲线图。该反应的热化学方程式为: 。
a、b两条曲线产生区别的原因很可能是 。
甲、乙、丙、丁、X是中学阶段的五种常见物质,它们的转化关系如下图所示(部分产物已略去):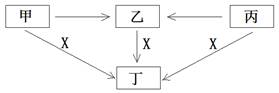
(1)若甲、乙、丙、丁均为化合物,且焰色反应均呈黄色。丙是淡黄色固体,常温下X是一种无色无味气体。则:
①甲和X生成丁的化学方程式为:
②丙和X生成丁的反应中还原剂是(填化学式),有0.2mol丁生成时,电子转移的数目是。
(2)若甲、乙、丙、丁都含有地壳中含量最多的金属元素,且丙受热时分解生成乙。X、丁溶液的焰色反应均为紫色(透过蓝色钴玻璃)。
①图中五个转化中属于氧化还原反应的数目是
| A.2 | B.3 | C.4 | D.5 |
②乙和X生成丁的离子方程式为。
③溶液中生成的丙能够净水,其原因是。
某混合物A,含有KAl(SO4)2、Al2O3和Fe2O3,实验小组利用A制备Al(OH)3的操作流程如下: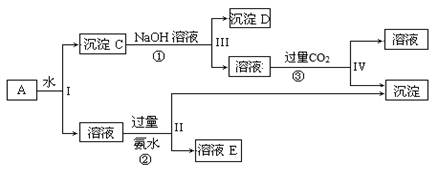
据此回答下列问题:
(1)I、II、III、IV四步中分离溶液和沉淀所采取的操作名称是,该实验操作所用到的玻璃仪器有。
(2)根据上述流程,写出D、E所含物质的化学式:
沉淀D;溶液E、。
(3)写出②、③反应的离子方程式:
②;③;
在100 mL MgCl2和AlCl3的混和溶液中,逐滴加入1 mol/L NaOH溶液直至过量,经测定,加入NaOH的物质的量和所得沉淀的物质的量的关系如下图所示,
则:
(1)图中C点表示加入mLNaOH,AB段发生的离子反应方程式。
(2)c(MgCl2)=mol·L—1
(3)图中线段OA︰AB=。
某大理石含有的主要杂质是氧化铁,以下是提纯该大理石的实验步骤:
(1)溶解大理石时,用硝酸而不用硫酸的原理是:。
(2)操作Ⅰ的目的是:,该反应的离子方程式是:。
(3)写出加入(NH4)2CO3所发生反应的离子方程式:,
滤液A的一种用途是。
有下列转化关系(反应条件略):
已知:① X、Y、Z、W均为氧化物。常态下,X是红棕色气体;Y能使澄清石灰水变浑浊但不能使品红溶液褪色。② 相对分子质量:甲﹤乙。③ 将甲的浓溶液露置在空气中一段时间,质量减小浓度降低;将乙的浓溶液露置在空气中一段时间,质量增加浓度降低。请填写下列空白:
(1)Z的化学式:。
(2)将乙的浓溶液露置在空气中一段时间,质量增加浓度降低,反映出乙的浓溶液具有性。利用这种性质可以进行项(填字母)实验操作。
a.钝化铁片b.检验Ba2+离子c.干燥氨气 d.干燥氯气
(3)在X和Z的反应中,被氧化的X与被还原的X的物质的量之比是:。
(4)W可用于工业制溴过程中吸收潮湿空气中的Br2 ,写出该反应的化学方式:。
(5)写出M与甲的浓溶液在加热条件下反应的化学方程式:。