(10分,每空2分)现要制取一些二氧化氮气体来做演示分子运动的实验。已知二氧化氮气体可以
通过铜和浓硝酸反应得到,其化学方程式为:Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O。二氧化氮是一种红棕色的气体,密度比空气大,能和水反应生成HNO3和NO气体,NO则为一种无色气体,难溶于水,一遇到O2就会变成NO2,NO和NO2都是大气污染物。现给出下列装置(A~G),请回答有关问题: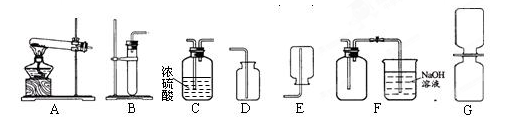
(1)制取一瓶干燥的二氧化氮气体时,所选择的装置依次为 (填序号);
(2)收集NO气体时应用_________________法;
(3)写出二氧化氮和水反应的化学方程式 ;
(4))用如上图G装置演示分子运动时,为了缩短演示的时间,NO2最好放在_________(选填“上”或“下”)面的集气瓶中,另一瓶是空气,抽去两瓶之间的玻璃片,可以观察到的现象是: 。
有A~E五种稀溶液,分别是稀盐酸、氢氧化钠溶液、氢氧化钙溶液、酚酞溶
液、碳酸钠溶液、氯化钠溶液中的一种,请根据以下实验现象回答问题。
已知:碳酸钠溶液呈碱性。
(1)将适量A分别滴入盛有少量B、C、D、E的试管中,实验记录如下:
| B |
C |
D |
E |
|
| A |
无明显变化 |
液体变红色 |
无明显变化 |
白色沉淀 |
C中溶液是,E中发生反应的化学方程式为。
(2)再将适量B分别滴加到上述实验后盛有C、D、E的试管中,C中液体由红色变为无
色,D中无明显变化,E中沉淀消失。
①B中溶液是,C中发生反应的化学方程式是。
②盛有E的试管中最终所得溶液中一定含有的溶质是。
(3)对还没有确定的液体,下列鉴别方法中,正确的是(填字母序号)。
A.分别滴加适量水 B.分别蒸发溶剂
C.分别滴加无色酚酞溶液 D.分别通入CO2后,再滴加稀盐酸
二氧化硫与二氧化碳具有某些相似的化学性质。为研究二氧化硫的性质,化学小组同学用如图所示装置进行实验。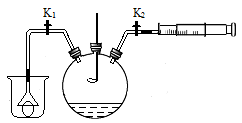
关闭K1、K2,将燃烧匙中硫粉在空气中点燃,迅速伸入如图所示瓶中,可以观察到火焰呈蓝紫色,则瓶内的气体是,硫燃烧反应的化学方程式是。瓶内的石蕊溶液由紫色变为红色,原因是。
(1)若只打开K1,烧杯内的兵乓球被吸在漏斗口,原因是。
(2)若注射器中盛有溶液A,只打开K2,可观察到的现象是,瓶内溶液变为蓝色,溶液A一定具有的性质是。
(3)若注射器中盛有澄清石灰水,打开K1、K2,向外拉注射器,可观察到澄清石灰水变浑浊,反应的化学方程式是。
物质在发生化学反应时要遵循质量守恒定律。甲、乙、丙、丁四组同学从不同的角度研究了质量守恒定律。
(1)甲组研究了反应:2H2+O2 2H2O,他们从该反应中获取的信息有:
2H2O,他们从该反应中获取的信息有:
①该反应的反应物是氢气和氧气;
②该化学反应的条件是点燃;
③在化学反应前后元素种类和原子个数不变;
④_________;⑤_________。
(2)乙、丙两组同学分别设计了如下实验,图中试剂混合前后物质的总质量分别表示为m(前)、m(后)。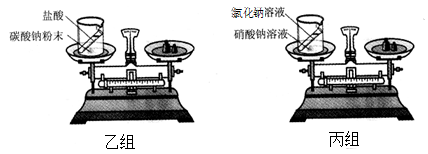
请根据图示回答:
乙组实验中,m(前)>m(后),原因是_______,若所用试剂不变,改进的方法是________;
丙组实验中,m(前)= m(后),乙组同学认为该实验不能验证质量守恒定律,原因是________。
(3)丁组同学研究了物质W的组成。一定条件下,W在密闭容器内发生反应前后各物质的质量如下图所示: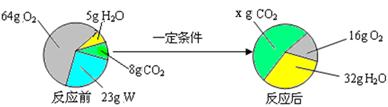
其中,x=g, W的化学式是。
嫩肉粉的主要成分是碳酸氢钠(NaHCO3),可破坏肉质纤维结构、促进肉类吸收水分,从而使肉质松软,达到鲜嫩爽滑的目的。小明发现将拌了嫩肉粉的肉类放到锅中加入食醋调味烧煮时产生了大量气体,她对此颇感兴趣,决定对其进行探究。
I. 小明对气体的成分进行了猜测:气体中除了醋酸气体和水蒸气之外,还可能含有气体A,A是。
Ⅱ. 小明对气体A的来源做了两种猜测:
猜测1:;
猜测2:气体A可能是由碳酸氢钠受热分解产生的。
针对以上猜测,小明设计了以下实验:
| 实验步骤 |
实验现象 |
|
| 实验1 |
||
| 实验2 |
取碳酸氢钠样品少许加入试管中,加热使之充分反应,并把产生的气体通入澄清石灰水 |
试管口出现小水珠,澄清石灰水变浑浊 |
实验结论:猜想①②都正确。
Ⅲ.实验2中,小明发现充分反应后,试管中仍留有一些白色粉末,他猜测可能是氢氧化钠或碳酸钠,请用物理、化学方法各一种进行鉴别。
(1)物理方法:。
(2)化学方法:。
氢氧化钠与盐酸的反应无明显现象,某化学兴趣小组为证明氢氧化钠与盐酸发生了化学反应,进行了如下的实验探究。
【实验探究一】小云在试管中加入约2mL稀氢氧化钠溶液,滴入2滴酚酞溶液,振荡,溶液变为红色。然后向该试管中滴加稀盐酸,观察到溶液,证明氢氧化钠与盐酸发生了反应,该反应的化学方程式为。
【反思评价】 小霞提出也可以使用石蕊试液代替无色酚酞进行上述实验。你认为(填“无色酚酞”或“石蕊试液”)更适合用于验证二者恰好完全反应,你的理由是。
【实验探究二】小兰同学将不同浓度的盐酸和NaOH溶液各10 mL混合,用温度计测定室温下混合前后温度的变化,并记录了每次混合前后温度的升高值△t(如下表)。
| 编号 |
盐酸 |
NaOH溶液 |
△t/℃ |
| 1 |
3.65﹪ |
2.00﹪ |
3.5 |
| 2 |
3.65﹪ |
4.00﹪ |
x |
| 3 |
7.30﹪ |
8.00﹪ |
14 |
表中x =。
【反思评价】某同学在没使用温度计的情况下,通过右图所示装置完成了实验。则该同学根据
判断NaOH溶液与稀盐酸发生了中和反应。但有同学认为单凭此现象不足以说明该反应放热,其理由是。
【拓展延伸】不是所有的碱与盐酸反应都无明显现象,例如(填一种碱)与盐酸反应就有明显的实验现象。